��Ŀ����
10�������������Ԫ�أ��Ǻϳ�Ѫ���ص���Ҫԭ�ϣ�ȱ�������ƶѪ���г��ϳ�����Ѫ������������������������������ʽC4H2O4Fe������������������������������������Ƭ���ȣ�ij��ѧ��ȤС��ͨ��ʵ�������������Ѫ���ɷֽ���̽�����ⶨFe2+�ĺ������ɹ�ѡ����Լ���˫��ˮ��KSCN��Һ�����ᡢBaCl2��Һ����֪KSCN�ɱ�˫��ˮ����������1���ɷ�̽����С���Ա��������������Ѫ�����������Ǻ�ɫ�ģ������ǵ�����ɫ�ģ���ͬѧ������ɽ�������̽����
| ʵ��̽�� | ʵ����������� | ���۷��� |
| ̽��һ | ��������ɫ��ĩ�ܽ���������Һ�У�ȡ����Һ2�ݣ� ��1�ݵμ�BaCl2��Һ��������ɫ�������ټ����ᣬ�����Ա仯�� ����1����Һ�ȵμ�KSCN��Һ�������Ա仯���ٵμ�˫��ˮ����μ�KSCN��Һ��Һ�����Ѫ��ɫ�� | ֤��������ɫ��ĩΪFeSO4 |
| ̽���� | ����ɫ�����гɷ�ĩ���μ����ᣬ�����Ա仯���ٵμ�KSCN��Һ������������ | ֤������ɫ���ʲ���Fe2O3�� |
��Ѫ����1Ƭ0.5�ˣ�$\stackrel{���ܽ�}{��}$��Һ$��_{��}^{����ɫ}$��Һ$\stackrel{������}{��}$���1L����Һ
�ٲ������Һ��ɫ�����A�����ţ��������ܵõ���Һ��

�ڼ�ͬѧ��Ϊ�������Һֱ�������ᾧ���ܵõ������������壬��������Ϊ���������ڼ��ȹ������ױ�����������ķ����Ǽ����������ۣ�С�����������ֽᾧĤʱֹͣ���ȣ�
����֪������м���������H2O2��Һ�������ǽ�Fe2+��ȫ������Fe3+��Ȼ���Ȳ��ò����������������ݲ�����Ŀ���dz�ȥ������H2O2��
��д��������з�����Ӧ�����ӷ���ʽ��2Fe2++H2O2+2H+=2Fe3++2H2O
��3���ⶨ����������Ѫ������Һ��Ũ��
������һ��������ֹ��ȷ���ʹ������ֹ��ȼƣ�����ͬ�����Ĺ����������䵽һ����Ũ�ȵμ�5mL 0.2mol•L-1 ����������ػ���Һ��������������Һ���õ��벻ͬ�������Ӧ������ǿ�ȣ���������������Һ��Ũ��Ϊ�����꣬�����Ϊ�����꣬��������ʵ����չ���������ͼ��
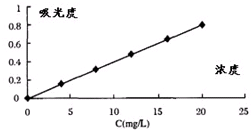
��ȡ����Һ10mL�μ�5mL 0.2mol•L-1 ����������ػ���Һ����ϡ����60mL��������ֹ��ȷ���ô���Һ�������Ϊ0.4������Ʒ����Ԫ�ص�����������12%��
����������KMnO4����Һ�ζ�������ȡ4.0g������������Ʒ������ˮ����������ϡ���ᣬ��0.2mol•L-1 KMnO4��Һ�ζ�������Һ��Fe2+ȫ��������ʱ������KMnO4��Һ���10.00mL��
��KMnO4��Һ������ʽ�ζ����У��յ����ɫ�仯��dz��ɫ���dz��ɫ
��Ҫ�ﵽ�õ�����Ч�������ò�Ѫ��ʱ��ע��ڷ�����Ӧͬʱ����ά����C��������ά����C���л�ԭ�ԣ���ֹFe2+��������
���� ��1��֤��������ɫ��ĩΪFeSO4��һ��֤������������ӣ���һ�ݼ���KSCN��Һ��ɫ���֣�����������⣬����KSCN��Һ����ɫ֤��ԭ��Һ��Ϊ�������ӣ�
��2���ٲ������Һ��ɫ����˳�ȥ�������ʲ������ܵõ���Һ��
����Һֱ�������ᾧ���ܵõ�����������������Ϊ���������ױ�������Ϊ��ֹ����Ӧ����������м��
�ۼ���������H2O2��Һ��Ϊ��������������Ϊ�����ӣ��Ȳ��ò����������������ݳ�ȥ�����������⣻
����������������Һ�б����������������������ӣ�
��3���������Ϊ0.4���������������Ũ��Ϊ10mg/L����Ʒ10mlϡ����60ml������ԭ��Һ����������Ũ��Ϊ60mg/L��0.5g��Ʒ������������60mg��
���������Һ����ǿ�������������ܣ������ü�ʽ�ζ���ʢ�ţ�������������Ϊdz��ɫ������������������Һ�ʻ�ɫ����ָʾ�ζ���Ӧ���յ㣻
�߷���ά����C����ʹʳ���е������ӻ�ԭ���������ӣ��������������գ�
��� �⣺��1����֤��������ɫ��ĩΪFeSO4����������ɫ��ĩ�ܽ���������Һ��ȡ����Һ2�ݣ������Ȼ�����Һ���ɲ���������İ�ɫ����֤������������ӣ���һ�ݼ���KSCN��Һ��ɫ���֣�����������⣬����KSCN��Һ����ɫ֤��ԭ��Һ��Ϊ�������ӣ�
�ʴ�Ϊ��KSCN��Һ��
��2���ٲ�Ѫ����1Ƭ0.5�ˣ��ܽ�õ���Һ��ɫ����˵õ���Һ��
�ʴ�Ϊ��A��
����Һֱ�������ᾧ���ܵõ������������壬��Ϊ�������Ӿ��л�ԭ�ԣ����������ڼ��ȹ������ױ��������ڼ�������������Ӧ�����������ۣ�С�����������ֽᾧĤʱֹͣ���ȣ�
�ʴ�Ϊ����Ϊ���������ڼ��ȹ������ױ����� �����������ۣ�С�����������ֽᾧĤʱֹͣ���ȣ�
�۲�����м���������H2O2��Һ��Ϊ��������������Ϊ�����ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O���Ȳ��ò����������������ݲ�����ȥ������H2O2��
�ʴ�Ϊ����Fe2+ ��ȫ������Fe3+����ȥ������H2O2��
����������������Һ�б����������������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��3���������Ϊ0.4���������������Ũ��Ϊ10mg/L����Ʒ10mlϡ����60ml������ԭ��Һ����������Ũ��Ϊ60mg/L��0.5g��Ʒ������������60mg����һ��������Ԫ�ص���������=$\frac{0.060g}{0.5g}$��100%=12%��
�ʴ�Ϊ��12%��
���������Һ����ǿ�������������ܣ������ü�ʽ�ζ���ʢ�ţ�Ӧ����ʽ�ζ���ʢ�ţ��յ����ɫ�仯��dz��ɫ��Һ�仯Ϊ��ɫ��Һ��
�ʴ�Ϊ���dz��ɫ���dz��ɫ��
��ά����C�л�ԭ�ԣ��ܷ���ά����C����ʹʳ���е������ӻ�ԭ���������ӣ��������������գ�
�ʴ�Ϊ��ά����C���л�ԭ�ԣ���ֹFe2+��������
���� ���⿼��ѧ�������ʵ���Ũ����Һ������ʵ��ԭ����ʵ����������⡢��ѧ���㡢�ζ�����ȣ��Ѷ��еȣ����ʵ��ԭ���ǽ���Ĺؼ�����Ҫѧ���߱���ʵ�Ļ���֪ʶ���ۺ�����֪ʶ�������⡢��������������

| A�� | ��������ڴ���Ƥ������ɫ�Լ�ƿ�� | |
| B�� | Ca��OH��2��Һ������ĥ�ڲ���������ɫ�Լ�ƿ�� | |
| C�� | NaOH��Һ����ڴ���Ƥ����ϸ�ڲ���ƿ�� | |
| D�� | NaOH����ʢ���ڴ���Ƥ����ϸ�ڲ���ƿ�� |
����ȡ�Ȼ�п��Ҫ������ͼ��
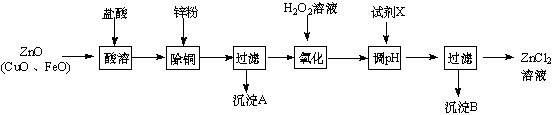
��֪��Zn���������������Al����������������ƣ�pH��11ʱZn��OH��2������NaOH��Һ����[Zn��OH��4]2-������г�����ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0mol•L-1���㣩��
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
��2������ͼ�У�Ϊ�˽�����Һ����ȣ��Լ�X������abc ��ѡ����ţ�a��ZnO��b��Zn��OH��2��c��Zn2��OH��2CO3��d��ZnSO4����pHӦ������3.2��pH��5.2��
��3���Ȼ�п�ܴ����ᣨ
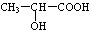 �����ɱ�������C6H8O4���;����ᣬ�������Ľṹ��ʽΪ
�����ɱ�������C6H8O4���;����ᣬ�������Ľṹ��ʽΪ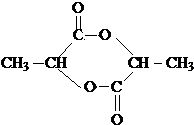 ��������Ľṹ��ʽΪ
��������Ľṹ��ʽΪ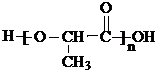 ��
������ȡ����п���ü��ܽ�{ZnO��s��+2NaOH��aq��+H2O��l���TNa2[Zn��OH��4]��aq��}��Ȼ�����ȡҺ��
��4����ʯī���缫���ʱ����������������ΪO2�������ĵ缫��ӦΪ[Zn��OH��4]2-+2e-=Zn+4OH-��
��5����п�̳����ü��ܣ������������ܺ��⣬��Ҫԭ��������ͭ���������������ڼ���Һ�У�
| A�� | 49������ | B�� | 0.8Ħ������ | ||
| C�� | 6������ | D�� | 6.02��1023 ������������� |
 ��1����ѧ�������о���������CH4��CO2��ת�������ã�
��1����ѧ�������о���������CH4��CO2��ת�������ã�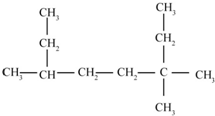 ������Ϊ3��3��6-��������
������Ϊ3��3��6-�������� 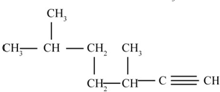 ������Ϊ3��6-����-1-��Ȳ
������Ϊ3��6-����-1-��Ȳ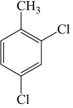 ��
��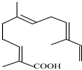 �������ʽΪC15H22O2��
�������ʽΪC15H22O2��