��Ŀ����
������һ�����������������Ź㷺���õĻ�ѧ���ʣ��������ھ�������������ˮ������������ҵ�������ΪƯ����Ŀǰ���õ��˹��Ʊ������ķ����У����ηŵ編���绯ѧ���������߷��ȣ����е绯ѧ�������豸���ף�ʹ��ά����ȫ�����ɳ����ɷִ������ص���õ��㷺���ã�ij����С��������ͼװ����PbO2��������Pt�缫Ϊ������ⱥ��K2SO4��Һ�Ʊ�O3�������õ������ⶨ�����IJ��ʣ�����֪���ʱ����������������O2�ĸ���Ӧ�������������ⶨ�Ĺ����в�����O2��KI��Ӧ ��
��������=
��100%
ʵ��������£�
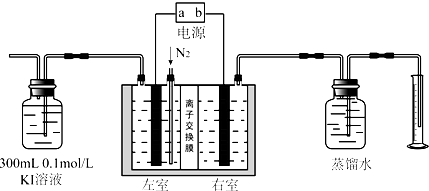
�ٰ���ͼ���Ӻ�װ�ã���������Ժ��ͨ��Դ��ʼ���з�Ӧ��
�ڵ��Ĺ�������1.5L/min�����ʹ���N2��ʹ������O3�ܹ���ȫ��KI��Һ���գ���Ӧ����O2���ɣ������Ǹù�������Һ����仯����
�۵��20min��ͨ����Ͳ��������в������������Ϊ224ml����ת��Ϊ��״������
�ܽ����������O3��300ml KI��Һȡ��30.00ml������2��0.1mol/L�ĵ�����Һ��ָʾ������0.01mol/L��Na2S2O3��Һ���еζ����������Na2S2O3��Һ�����Ϊ31.00ml������֪��Ӧ�Ļ�ѧ����ʽΪ��I2+2Na2S2O3=Na2S4O6+2NaI ��
��1�����Ҳ���������Ϊ ���ѧʽ����д�����ҷ����ĵ缫��Ӧ����ʽ ��
��2��д��KI��Һ����O3�Ļ�ѧ����ʽ ��
��3����ʵ������й���N2�����ʲ��ܹ��죬������̫��ⶨ�������IJ��ʽ�ƫ �����С����������ʵ���������ݣ���װ�ò��������IJ���Ϊ ��
��������=
| ʵ�ʲ��� |
| ���۲��� |
ʵ��������£�
�ٰ���ͼ���Ӻ�װ�ã���������Ժ��ͨ��Դ��ʼ���з�Ӧ��
�ڵ��Ĺ�������1.5L/min�����ʹ���N2��ʹ������O3�ܹ���ȫ��KI��Һ���գ���Ӧ����O2���ɣ������Ǹù�������Һ����仯����
�۵��20min��ͨ����Ͳ��������в������������Ϊ224ml����ת��Ϊ��״������
�ܽ����������O3��300ml KI��Һȡ��30.00ml������2��0.1mol/L�ĵ�����Һ��ָʾ������0.01mol/L��Na2S2O3��Һ���еζ����������Na2S2O3��Һ�����Ϊ31.00ml������֪��Ӧ�Ļ�ѧ����ʽΪ��I2+2Na2S2O3=Na2S4O6+2NaI ��
��1�����Ҳ���������Ϊ
��2��д��KI��Һ����O3�Ļ�ѧ����ʽ
��3����ʵ������й���N2�����ʲ��ܹ��죬������̫��ⶨ�������IJ��ʽ�ƫ

���㣺���ԭ��
ר�⣺�绯ѧר��
��������1����ͼ����ʾ��֪������Ϊ�����ң���ⱥ��K2SO4��Һ����Ӧ��ΪH+�ŵ磬������������Ӧ�ò���H2������Ϊ�����ң���������O3���缫��ӦΪ3H2O-6e=O3+6H+��
��2��KI��Һ��Ϊ����Һ����O3��������I-�Ļ�ԭ�ԣ����Է����Ļ�ѧ��Ӧ����ʽΪO3+2KI+H2O=O2+I2+2KOH��
��3����ͨ��N2�����ʹ��죬O3��KI��Ӧ����֣������I2��ƫС�������O3���ʾͻ�ƫС��������������22.4ml 0.001mol H2��֪�������е���ת������Ϊ 0.002 mol�������Ͽ�����O3 0.001��3 mol��ʵ���ϲ�����O3����ͨ�����ĵ�Na2S2O3��O3֮��Ĺ�ϵ�����Ϊ1.55��10-4mol�����ǿ��������Ϊ46.5%��
��2��KI��Һ��Ϊ����Һ����O3��������I-�Ļ�ԭ�ԣ����Է����Ļ�ѧ��Ӧ����ʽΪO3+2KI+H2O=O2+I2+2KOH��
��3����ͨ��N2�����ʹ��죬O3��KI��Ӧ����֣������I2��ƫС�������O3���ʾͻ�ƫС��������������22.4ml 0.001mol H2��֪�������е���ת������Ϊ 0.002 mol�������Ͽ�����O3 0.001��3 mol��ʵ���ϲ�����O3����ͨ�����ĵ�Na2S2O3��O3֮��Ĺ�ϵ�����Ϊ1.55��10-4mol�����ǿ��������Ϊ46.5%��
���
�⣺��1����ͼ����ʾ��֪������Ϊ�����ң���ⱥ��K2SO4��Һ����Ӧ��ΪH+�ŵ磬������������Ӧ�ò���H2������Ϊ�����ң���������O3���缫��ӦΪ3H2O-6e=O3+6H+���ʴ�Ϊ��H2�� 3H2O-6e=O3+6H+��
��2��KI��Һ��Ϊ����Һ����O3��������I-�Ļ�ԭ�ԣ����Է����Ļ�ѧ��Ӧ����ʽΪ��O3+2KI+H2O=O2+I2+2KOH���ʴ�Ϊ��O3+2KI+H2O=O2+I2+2KOH��
��3����ͨ��N2�����ʹ��죬O3��KI��Ӧ����֣������I2��ƫС�������O3���ʾͻ�ƫС��
������������22.4ml ��0.001mol H2��֪�������е���ת������Ϊ0.001mol��2=0.002 mol�����ݵ�ʧ�����غ������Ͽ�����O3
=
��10-3mol��ʵ���ϲ�����O3��
����O3+2KI+H2O=O2+I2+2KOH��I2+2Na2S2O3=Na2S4O6+2NaI �ó�
O3 ��I2 ��2Na2S2O3
1 2
1.55��10-4mol 0.01mol/L��0.031L=3.1��10-4mol
���dz�����Ϊ
��100%=46.5%���ʴ�Ϊ��ƫС��46.5%��
��2��KI��Һ��Ϊ����Һ����O3��������I-�Ļ�ԭ�ԣ����Է����Ļ�ѧ��Ӧ����ʽΪ��O3+2KI+H2O=O2+I2+2KOH���ʴ�Ϊ��O3+2KI+H2O=O2+I2+2KOH��
��3����ͨ��N2�����ʹ��죬O3��KI��Ӧ����֣������I2��ƫС�������O3���ʾͻ�ƫС��
������������22.4ml ��0.001mol H2��֪�������е���ת������Ϊ0.001mol��2=0.002 mol�����ݵ�ʧ�����غ������Ͽ�����O3
| 0.002 |
| 6 |
| 1 |
| 3 |
����O3+2KI+H2O=O2+I2+2KOH��I2+2Na2S2O3=Na2S4O6+2NaI �ó�
O3 ��I2 ��2Na2S2O3
1 2
1.55��10-4mol 0.01mol/L��0.031L=3.1��10-4mol
���dz�����Ϊ
| 1.55��10 -4 | ||
|
�����������ۺϿ�����ԭ���������õζ�������ʣ������ڵ缫����ʽ�Ŀ���Ͱ�����ʽ���м��㣬ע����յ缫��Ӧ���жϺ���д�Լ����ݷ���ʽ��ϵ����ϵ���㣬������ע����᷽����

��ϰ��ϵ�д�
�����Ŀ
��һ�������´��ڷ�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����������Ӧ���ȣ�����������ͬ��2L���ݾ��ȣ������û�������������ܱ��������ڢ��г���1 molCO��1molH2O���ڢ��г���1 molCO2�� 1 mol H2��d�ڢ��г���2 mol��2 mol H2O.700�������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ���ǣ�������
| A��������������Ӧ������ͬ |
| B���������з�Ӧ��ƽ�ⳣ����ͬ |
| C����������CO�����ʵ������������е��� |
| D����������CO��ת��������������CO2��ת���ʺ�С��1 |
Al��Ͷ��ij��ɫ�������Һ�в���H2����ԭ��Һ�е����������ȷ���ǣ�������
| A��H+��Ca2+��Na+��CO32- |
| B��Na+��Mg2+��OH-��Cl- |
| C��Fe2+��Mg2+��Cl-��H+ |
| D��Ba2+��Cl-��OH-��NO3- |
���и�����ɫ��Һ�У����������ܴ���������ǣ�������
| A��K+�� Na+�� Cl-��NO3- |
| B��Cu2+�� H+�� HCO3-�� Cl- |
| C��Na+�� Ba2+�� Cl-�� SO42- |
| D��Fe2+�� H+�� NO3-�� ClO- |
�����йػ�ѧʵ������С��ȡ��롰��˵����ȷ���ǣ�������
| A��������ؼ����Ʊ�����������ˮ���ռ����������ȳ���ƾ��ƣ����Ƴ����� |
| B�����Թܼ���ʱ���ȹ̶��ֲ����ȣ�����Թ����ؾ��ȼ��� |
| C���ڲⶨ��Һ��pHʱ����������ˮʪ���ò�����պȡ��Һ������ֽ�в��������ɫ���Ƚ� |
| D����ȼ��ȼ�����壨��H2��CO��CH4��ʱ���ȼ������崿�ȣ����ȼ |
����ͬ�¶��£���֪2H2��g��+O2��g��=2H2O��g����H1�� 2H2��g��+O2��g��=2H2O��l����H2��H2��g��+
O2��g��=H2O��l����H3�����H1����H2����H3��С��ϵΪ��������
| 1 |
| 2 |
| A����H1=��H2=��H3 |
| B��2��H3=��H2����H1 |
| C����H3����H2����H1 |
| D��2|��H3|=|��H2|��|��H1| |
���и��������У���Ϊ��Ӧ������������ͬ��������ͬ��ѧ��Ӧ���ǣ�������
��C��O2 ��Na��O2 ��Fe��Cl2 ��AlCl3��Һ��NaOH��Һ��CO2��NaOH��Һ ��Fe�����ᣮ
��C��O2 ��Na��O2 ��Fe��Cl2 ��AlCl3��Һ��NaOH��Һ��CO2��NaOH��Һ ��Fe�����ᣮ
| A�������� | B�����ۢ��� |
| C�����ۢ��� | D�������� |

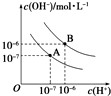 ��֪ˮ��25�棨A����T�棨B��ʱ�������ƽ��������ͼ��ʾ��
��֪ˮ��25�棨A����T�棨B��ʱ�������ƽ��������ͼ��ʾ��