题目内容
9.下列电离方程式正确的是( )| A. | NaHS 溶于水:NaHS═Na++HS- HS-?H++S2- | |
| B. | (NH4)2SO4溶于水:(NH4)2SO4?2NH4++SO42- | |
| C. | 磷酸溶于水中:H3PO4═3H++PO43- | |
| D. | Al(OH)3的电离:Al(OH)3=Al3++3OH- |
分析 先判断电解质的强弱,强电解质完全电离,弱电解质存在电离平衡,结合离子的符合、电荷守恒、原子守恒判断电离方程式.
解答 解:A.NaHS为强电解质,电离方程式为NaHS═Na++HS-,且HS-?H++S2-存在电离平衡,故A正确;
B.(NH4)2SO4为强电解质,电离方程式为(NH4)2SO4=2NH4++SO42-,故B错误;
C.磷酸为弱电解质,存在电离平衡,电离方程式为H3PO4?H++H2PO4-,以第一步电离为主,故C错误;
D.Al(OH)3为弱电解质,存在电离平衡,电离方程式为Al(OH)3?Al3++3OH-,故D错误;
故选A.
点评 本题考查电离方程式的书写,为高频考点,把握电解质的强弱、电离方程式的书写方法为解答的关键,侧重分析与应用能力的考查,注意多元弱酸与弱碱的电离方程式书写方法不同,题目难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
20. (1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
(1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
已知反应①中相关的化学键键能数据如表:
由此计算△H1=-99kJ•mol-1.已知△H2=-58kJ•mol-1,则△H3=+41kJ•mol-1.
 (1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
(1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
已知反应①中相关的化学键键能数据如表:
| 化学键 | H-H | C-O | C-O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | 1075 | 465 | 413 |
17.下列关于物质“反应程度”的说法正确的是( )
| A. | 一定条件下,2mol SO2与足量O2反应可得到2mol SO3 | |
| B. | 含4mol HCl的浓盐酸与足量的MnO2加热反应可制备1mol Cl2 | |
| C. | 10mL 18.0mol/L H2SO4与足量铜加热反应可制备0.09mol SO2 | |
| D. | 一定条件下,1mol N2与3mol H2反应可制备1.0 mol NH3 |
14.下列各组物质混合后,不能生成NaOH的是( )
| A. | Na和H2O | B. | Na2O和H2O | ||
| C. | Ca(OH)2和Na2CO3溶液 | D. | Ca(OH)2和NaCl溶液 |
1.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 酸性溶液中:Na+、K+、MnO4-、CO32- | |
| B. | 碱性溶液中:Na+、ClO-、SO42-、I- | |
| C. | 0.1mol•L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 0.1mol•L-1FeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
13.某元素的原子核外有三个电子层,其最外层电子数是次外层电子数的一半,则此元素是( )
| A. | S | B. | C | C. | Si | D. | Cl |
14.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol Na2O2与足量的潮湿的二氧化碳反应转移的电子数为0.1NA | |
| B. | 1 mol镁与足量O2或N2反应生成MgO或Mg3N2失去电子分别为2NA和3NA | |
| C. | 含NA个Na+的Na2O2溶于1 L水中,Na+的物质的量浓度为1 mol/L | |
| D. | 某密闭容器中盛有0.2 molN2和0.3 molH2,在一定条件下充分反应,转移电子的数目为0.6 NA |
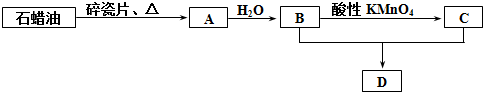
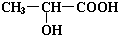 ;
;