题目内容
下列离子方程式书写错误的是( )
| A、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、澄清石灰水与盐酸混合:OH-+H+=H2O |
| C、NaOH溶液与CuSO4溶液反应2OH-+Cu2+=Cu(OH)2↓ |
| D、铜与 AgNO3溶液反应 Cu+2Ag+=2Ag+Cu2+ |
考点:离子方程式的书写
专题:
分析:A.铁与稀盐酸反应生成氯化亚铁,不会生成氯化铁;
B.澄清石灰水中,氢氧化钙需要写成离子形式,反应实质为氢离子与氢氧根离子反应生成水;
C.氢氧化钠与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠;
D.铜活泼性大于银,铜与硝酸银反应生成银单质和硝酸铜.
B.澄清石灰水中,氢氧化钙需要写成离子形式,反应实质为氢离子与氢氧根离子反应生成水;
C.氢氧化钠与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠;
D.铜活泼性大于银,铜与硝酸银反应生成银单质和硝酸铜.
解答:
解:A.铁与稀盐酸反应生成亚铁离子,正确的离子方程式为:Fe+2H+=Fe2++H2↑,故A错误;
B.澄清石灰水与盐酸混合,反应生成氯化钙和水,反应的离子方程式为:OH-+H+=H2O,故B正确;
C.NaOH溶液与CuSO4溶液反应生成氢氧化铜沉淀,反应的离子方程式为:2OH-+Cu2+=Cu(OH)2↓,故C正确;
D.铜与AgNO3溶液发生置换反应生成银单质,反应的离子方程式为:Cu+2Ag+=2Ag+Cu2+,故D正确;
故选A.
B.澄清石灰水与盐酸混合,反应生成氯化钙和水,反应的离子方程式为:OH-+H+=H2O,故B正确;
C.NaOH溶液与CuSO4溶液反应生成氢氧化铜沉淀,反应的离子方程式为:2OH-+Cu2+=Cu(OH)2↓,故C正确;
D.铜与AgNO3溶液发生置换反应生成银单质,反应的离子方程式为:Cu+2Ag+=2Ag+Cu2+,故D正确;
故选A.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等),试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
在相同的温度和压强下,下列气体的密度最小的是( )
| A、CO2 |
| B、H2 |
| C、O2 |
| D、Cl2 |
如果a g某气体中含有该气体的分子数为b,则c g该气体在标准状况下的体积是(各选项中NA为阿伏加德罗常数)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列电离方程式不正确的是( )
| A、CaCl2=Ca2++2Cl- |
| B、NaHSO4=Na+H++SO 42- |
| C、HNO3=H++NO 3- |
| D、KHCO3=K++H++CO 32- |
按照下列分类方式可以将NaHCO3和KHSO4归为一类的是( )
| A、强碱 | B、酸式盐 | C、氧化物 | D、酸 |
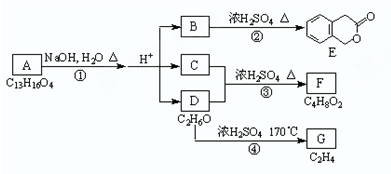
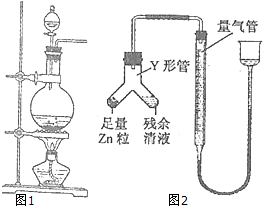 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1示).
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1示).