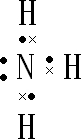题目内容
根据下列框图,有关说法正确的是( )
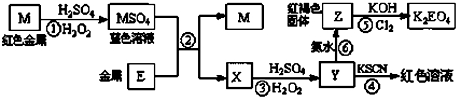

| A、M、E都是第四周期中的过渡元素,E的金属活动性比M的金属活动性强,E3+的氧化性比M2+的氧化性弱 | B、反应⑤的离子方程式可表示为:2E(OH)3+3Cl2+6H2O═3EO42-+6Cl-+12H+ | C、反应①、②、③、⑤都属于氧化还原反应,且在反应①和③中硫酸仅表现了酸性 | D、用K2EO4、Zn可制成一种高能电池,该电池中负极的电极反应式为:EO42-+4H2O+3e-═E(OH)3+5OH- |
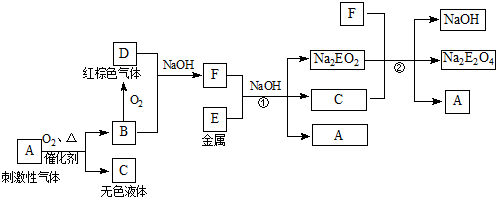
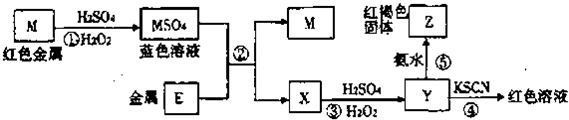
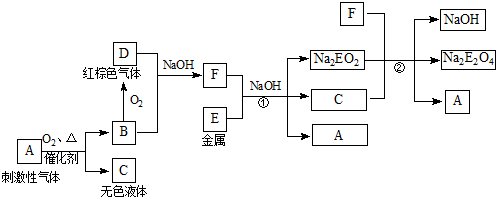
分析:流程分析可知,M为铜,在酸性溶液中被过氧化氢氧化为铜盐溶液CuSO4,依据Y加入KSCN溶液血红色说明是Fe3+离子,和氨水反应生成红褐色沉淀氢氧化铁;说明X为亚铁离子形成的硫酸亚铁溶液,推断E为Fe,则X为FeSO4,Y为Fe2(FeSO4)3,Z为Fe(OH)3,
A.Fe2+的氧化性比Cu2+的氧化性弱,但Fe3+的氧化性比Cu2+强,
B.Fe(OH)3可被氯气氧化生成高铁酸钾;
C.①和③中硫酸都只表现了酸性;
D.负极发生氧化反应.
A.Fe2+的氧化性比Cu2+的氧化性弱,但Fe3+的氧化性比Cu2+强,
B.Fe(OH)3可被氯气氧化生成高铁酸钾;
C.①和③中硫酸都只表现了酸性;
D.负极发生氧化反应.
解答:解:流程分析可知,M为铜,在酸性溶液中被过氧化氢氧化为铜盐溶液CuSO4,依据Y加入KSCN溶液血红色说明是Fe3+离子,和氨水反应生成红褐色沉淀氢氧化铁;说明X为亚铁离子形成的硫酸亚铁溶液,推断E为Fe,则X为FeSO4,Y为Fe2(FeSO4)3,Z为Fe(OH)3,
A.Fe2+的氧化性比Cu2+的氧化性弱,但Fe3+的氧化性比Cu2+强,如2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.Fe(OH)3可被氯气氧化生成高铁酸钾,反应在碱性条件下进行,不可能生成H+,应为2E(OH)3+3Cl2+12OH-═3EO42-+6Cl-+6H2O,故B错误;
C.①②⑤都有单质参加反应,③有过氧化氢参加反应,则一定为氧化还原反应,①和③中硫酸都只表现了酸性,表现氧化性的为过氧化氢,故C正确;
D.负极发生氧化反应,应是锌失电子被氧化,故D错误.
故选C.
A.Fe2+的氧化性比Cu2+的氧化性弱,但Fe3+的氧化性比Cu2+强,如2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.Fe(OH)3可被氯气氧化生成高铁酸钾,反应在碱性条件下进行,不可能生成H+,应为2E(OH)3+3Cl2+12OH-═3EO42-+6Cl-+6H2O,故B错误;
C.①②⑤都有单质参加反应,③有过氧化氢参加反应,则一定为氧化还原反应,①和③中硫酸都只表现了酸性,表现氧化性的为过氧化氢,故C正确;
D.负极发生氧化反应,应是锌失电子被氧化,故D错误.
故选C.
点评:本题考查无机物的推断,侧重于学生的分析能力的考查,较为综合,涉及氧化性的强弱以及电化学知识,难度中等,注意根据物质的颜色作为本题的突破口.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目