题目内容
16.取10.6g Na2CO3溶于水配成100ml溶液,求:(1)Na2CO3的物质的量
(2)所得Na2CO3溶液的物质的量浓度
(3)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.4mol/L,求加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)
分析 (1)根据n=$\frac{m}{M}$计算Na2CO3的物质的量;
(2)根据c=$\frac{n}{V}$计算碳酸钠的物质的量浓度;
(3)根据稀释定律C浓V浓=C稀V稀计算稀释后溶液的体积,进而计算加入蒸馏水的体积.
解答 解:(1)n(Na2CO3)=$\frac{10.6g}{106g/mol}$=0.1mol,
答:碳酸钠的物质的量为0.1mol;
(2)c(Na2CO3)=$\frac{0.1mol}{0.1L}$=1mol/L,
答:碳酸钠溶液的物质的量浓度为1mol/L;
(3)根据稀释定律,稀释后溶液的体积为$\frac{0.02L×1mol/L}{0.4mol/L}$=0.05L,则需要加入蒸馏水的体积为50mL-20mL=30mL,
答:需要加入蒸馏水的体积为30mL.
点评 本题考查物质的量浓度有关计算,理解物质的量浓度并能灵活应用,有利于基础知识的巩固.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
6.不能用来说明金属X比金属Y还原性强的是( )
| A. | 把X和Y组成的合金放于潮湿的空气中,X先被腐蚀 | |
| B. | X原子最外层电子数比Y原子最外层电子数少 | |
| C. | X能从Y的盐溶液中把Y置换出来 | |
| D. | X的最高价氧化物的水化物碱性比Y的强 |
7.下列有关有机物分离提纯的方法正确的是( )
| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出I2 | |
| B. | 乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 | |
| C. | 乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶,再干燥 | |
| D. | 除去乙醇中的微量水可加入金属钠,使其完全反应 |
4.只用下列试剂中的一种就能鉴别AgNO3、Na2CO3、K2SO4三种溶液,则该试剂是( )
| A. | KNO3溶液 | B. | Na2SO4溶液 | C. | NaOH溶液 | D. | 稀HCl |
11.下列反应不属于氧化还原反应的是( )
| A. | CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 | B. | NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl | ||
| C. | CuSO4+Zn=ZnSO4+Cu | D. | 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
1.下列解释事实的方程式正确的是( )
| A. | 将NO2通入水中,红棕色消失:3NO2+H2O═2HNO3+O2 | |
| B. | 向含有Hg2+的废水中加入Na2S 产生沉淀:Hg2++S2-═Hg+S↓ | |
| C. | Na 与水反应产生气体:2Na+H2O═2Na++2OH-+H2↑ | |
| D. | 向燃煤中加入石灰石可减少 SO2的排放:2CaCO3+O2+2SO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+2CO2 |
8.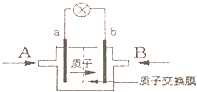 一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )
一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )
 一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )
一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )| A. | A处通氧气,B处通乙醇 | |
| B. | 电池工作时电子由a极沿导线经灯泡再到b极 | |
| C. | 电池正极的电极反应为:O2+2H2O+4e-=4OH- | |
| D. | 若用这种电池作电源保护金属铁,则a电极连接石墨,b连接铁 |
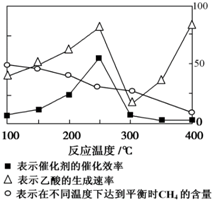 甲烷既是一种清洁能源,也是一种重要的化工原料.用催化剂可以将CO2和CH4直接转化成乙酸,反应方程式为:CO2(g)+CH4(g)?CH3COOH(g).
甲烷既是一种清洁能源,也是一种重要的化工原料.用催化剂可以将CO2和CH4直接转化成乙酸,反应方程式为:CO2(g)+CH4(g)?CH3COOH(g).