题目内容
15.下列实验设计能完成或实验结论合理的( )| 操作及现象 | 结 论 | |
| A | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| B | 向硅酸钠溶液中,滴入硫酸 | 可以验证S的氧化性强于Si |
| C | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| D | 向含有少量FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液 | 除去FeCl2溶液中的FeBr2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.测定溶液pH值时不能用蒸馏水润湿pH试纸,否则会导致溶液浓度降低;
B.非金属的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
C.二氧化硫具有还原性,溴具有氧化性,二者易发生氧化还原反应生成HBr和硫酸;
D.亚铁离子还原性大于溴离子.
解答 解:A.测定溶液pH值时不能用蒸馏水润湿pH试纸,否则会导致溶液浓度降低,则测定的pH值可能发生变化,测定结果可能偏低也可能不变,如测定强酸强碱盐溶液pH与溶液浓度无关,则测定结果不变,故A错误;
B.非金属的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,向硅酸钠溶液中,滴入硫酸生成硅酸,说明硫酸酸性大于硅酸,硫酸、硅酸都是非金属的最高价氧化物的水化物,所以可以比较非金属性强弱,故B正确;
C.二氧化硫具有还原性,溴具有氧化性,二者易发生氧化还原反应生成HBr和硫酸,该反应中二氧化硫体现还原性而不是漂白性,故C错误;
D.亚铁离子还原性大于溴离子,所以加入氯水后先氧化亚铁离子生成铁离子,然后氧化溴离子生成溴,所以不能实现实验目的,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及溶液pH值的测定、非金属性强弱判断、二氧化硫性质、氧化还原反应等知识点,侧重考查学生实验操作、实验评价和分析能力,明确实验原理、实验操作方法、元素化合物性质是解本题关键,注意D选项中离子反应先后顺序,为易错点.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
6.向下列溶液中逐滴加入NaOH溶液至过量,先有白色沉淀生成,然后沉淀又消失的是( )
| A. | CuCl2溶液 | B. | AlCl3溶液 | C. | MgCl2溶液 | D. | BaCl2溶液 |
3.下列说法中,正确的是( )
| A. | 钠和氢气分别在氯气中燃烧,都产生白色烟雾 | |
| B. | 铜丝在氯气中燃烧,生成蓝色的氯化铜 | |
| C. | 液氯和氯水中滴入硝酸银溶液均会产生白色沉淀 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液后溶液呈红色 |
10.下列反应的能量变化与其他三项不相同的是( )
| A. | 甲烷燃烧 | B. | 碳酸钙高温分解 | ||
| C. | 锌片与稀硫酸反应 | D. | 钠与冷水反应 |
20.在无土栽培中,需配制一定组成的植物营养液.已知某植物营养液的配方为0.6mol KCl、0.4mol K2SO4、0.20mol ZnSO4和1LH2O.若以KCl、K2SO4、ZnCl2和1LH2O为原料配得相同组成的营养液,需三种溶质的物质的量为( )
| A. | 0.20 mol、0.60 mol、0.20mol | B. | 0.30 mol、0.60 mol、0.10 mol | ||
| C. | 0.40 mol、0.60 mol、0.10 mol | D. | 0.20 mol、0.10mol、0.60 mol |
7.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,80 g SO3所占的体积约为22.4 L | |
| B. | 常温常压下,1.6 gO2和O3混合气体中质子总数为0.8NA | |
| C. | 0.1 mol甲基(-CH3)所含电子数为NA | |
| D. | 在熔融状态下,1 mol NaHSO4完全电离出的阳离子数目为2NA |
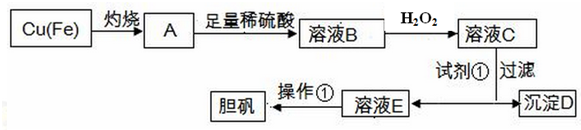
9.工业上利用废铜屑制备胆矾的工业流程如下:
已知:
请回答:
(1)加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)检验溶液B中Fe3+的方法是向溶液中加入KSCN溶液,然后观察现象,若溶液变红色,说明溶液中存在Fe3+,否则没有铁离子.
(3)利用试剂①调节溶液的pH至3.7-5.2,试剂①的化学式CuO或Cu(OH)2或Cu2(OH)2CO3.
(4)常温下,若溶液C中金属离子均为1mol•L-1,Ksp[Fe(OH)3]=4.0×10-36,Ksp[Cu(OH)2]=2.2×10-20.控制pH=4,溶液中c(Fe3+)=4.0×10-8,此时无Cu(OH)2沉淀生成(填“有”或“无”).
(5)操作①为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(6)测定溶液E中Cu2+浓度的方法为:准确量取V1 mL溶液E于锥形瓶中,调节pH=3~4,加入过量KI,充分反应后,滴加2滴淀粉溶液,再慢慢滴加c mol/LNa2S2O3标准溶液至恰好完全反应,消耗Na2S2O3标准溶液V2 mL.
已知:2Cu2++4I-=2CuI↓+I22S2O32-+I2=S4O62-+2I-
①“恰好反应”时溶液的颜色变化为蓝色变为无色.
②Cu2+的物质的量浓度为$\frac{c{V}_{2}}{{V}_{1}}$mol/L(用V1、V2、c表示).

已知:
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.8 | 6.3 | 5.2 |
| 完全沉淀的pH | 3.0 | 8.3 | 6.7 |
(1)加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)检验溶液B中Fe3+的方法是向溶液中加入KSCN溶液,然后观察现象,若溶液变红色,说明溶液中存在Fe3+,否则没有铁离子.
(3)利用试剂①调节溶液的pH至3.7-5.2,试剂①的化学式CuO或Cu(OH)2或Cu2(OH)2CO3.
(4)常温下,若溶液C中金属离子均为1mol•L-1,Ksp[Fe(OH)3]=4.0×10-36,Ksp[Cu(OH)2]=2.2×10-20.控制pH=4,溶液中c(Fe3+)=4.0×10-8,此时无Cu(OH)2沉淀生成(填“有”或“无”).
(5)操作①为蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(6)测定溶液E中Cu2+浓度的方法为:准确量取V1 mL溶液E于锥形瓶中,调节pH=3~4,加入过量KI,充分反应后,滴加2滴淀粉溶液,再慢慢滴加c mol/LNa2S2O3标准溶液至恰好完全反应,消耗Na2S2O3标准溶液V2 mL.
已知:2Cu2++4I-=2CuI↓+I22S2O32-+I2=S4O62-+2I-
①“恰好反应”时溶液的颜色变化为蓝色变为无色.
②Cu2+的物质的量浓度为$\frac{c{V}_{2}}{{V}_{1}}$mol/L(用V1、V2、c表示).