题目内容
5.亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2═LiNH2+LiH;则下列有关说法正确的是( )| A. | Li2NH中N的化合价是-1 | B. | 此法储氢和钢瓶储氢的原理相同 | ||
| C. | H+与H -的离子半径均比Li+大 | D. | 该反应中H2既是氧化剂又是还原剂 |
分析 A.Li2NH中H元素的化合价是+1,氮元素的化合价为-3;
B.钢瓶储氢是物理过程;
C.离子核外电子层数越多,半径越大;
D.LiNH2中氮元素的化合价为-3,H元素的化合价是+1;LiH中H元素的化合价是-1,可以从化合价变化的角度来判断氧化还原反应的有关概念.
解答 解:A.Li2NH中氮元素的化合价为-3,故A错误;
B.钢瓶储氢是物理过程,而该方法为化学方法,故B错误;
C.Li+核外有一个电子层,H+核外无电子,离子核外电子层数越多,半径越大,故Li+半径大于H+,故C错误;
D.反应物H2中的氢元素的化合价为0价,反应后生成LiNH2中H元素的化合价是+1,LiH中H元素的化合价是-1,所以H2既是氧化剂又是还原剂,故D正确.
故选D.
点评 本题考查氧化还原反应的有关概念,离子半径的大小比较等问题,做题注意从化合价变化的角度判断氧化剂、还原剂的等概念,注意离子半径大小比较的方法,注重基础知识的积累.

练习册系列答案
相关题目
13.下列溶液中,氯离子的物质的量浓度是3mol•L-1的是( )
| A. | 200mL 3mol•L-1 NaClO3溶液 | B. | 100mL 2mol•L-1 FeCl3溶液 | ||
| C. | 150mL 3mol•L-1 KCl溶液 | D. | 150mL 1mol•L-1 MgCl2溶液 |
17. 如图为元素周期表短周期的一部分,Z原子的电子层数为n,最外层电子数为2n+1.下列叙述错误的是( )
如图为元素周期表短周期的一部分,Z原子的电子层数为n,最外层电子数为2n+1.下列叙述错误的是( )
 如图为元素周期表短周期的一部分,Z原子的电子层数为n,最外层电子数为2n+1.下列叙述错误的是( )
如图为元素周期表短周期的一部分,Z原子的电子层数为n,最外层电子数为2n+1.下列叙述错误的是( )| A. | X和Z氢化物的热稳定性和还原性均依次减弱 | |
| B. | R、W和氢三种元素形成的阴离子有2种以上 | |
| C. | RY2分子中每个原子的最外层均为8电子结构 | |
| D. | R、Y、Z的最高价氧化物对应的水化物的酸性依次增强 |
10.标准状况下,若2.8LO2含有n个O2分子,则阿伏加德罗常数为( )
| A. | n/8 | B. | n/16 | C. | 8n | D. | 16n |
15.目前国际空间站处理CO2废气涉及的反应为CO2+4H2$\stackrel{钌催化剂}{?}$CH4+2H2O.该反应的下列说法正确的是( )
| A. | 钌催化剂能加快该反应的速率 | B. | 升高温度能减慢该反应的速率 | ||
| C. | 达到平衡时,CO2能100%转化为CH4 | D. | 达到平衡时,反应速率:v(正)=v(逆)=0 |
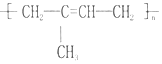 的名称聚2-甲基-1,3-丁二烯,其单体的结构简式CH2═C(CH3)CH═CH2.
的名称聚2-甲基-1,3-丁二烯,其单体的结构简式CH2═C(CH3)CH═CH2.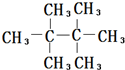 .
. .
. .
.