题目内容
有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20.其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1.B和D也属同一族,它们原子最外层的p电子数是s电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.回答下列问题:
(1)A是 .(填元素符号)
(2)写出C元素基态原子的电子排布式 ,该元素位于元素周期表的 区(填s p d ds f)
(3)写出C E两元素的最高价氧化物的水化物相互反应的离子方程式:
(4)元素B与D的电负性的大小关系是 (用元素符号填空,下同),C与E的第一电离能的大小关系是 .
(5)B位于周期表的第 周期,第 族;其原子结构示意图为 .
(1)A是
(2)写出C元素基态原子的电子排布式
(3)写出C E两元素的最高价氧化物的水化物相互反应的离子方程式:
(4)元素B与D的电负性的大小关系是
(5)B位于周期表的第
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,B和D元素原子的最外层电子数相同,二者处于同主族,且它们原子最外层的p电子数是s电子数的两倍,则最外层含有6个电子,则B为氧元素、D为硫元素;
C、E是金属元素,A和E原子的最外层电子排布为ns1,则原子的最外层电子都只有一个电子,二者处于ⅠA族,结合原子序数可知,E为K元素、A为氢元素;
C元素原子的最外层电子数是S元素原子最外层电子数的一半,即C为Al,据此解答.
C、E是金属元素,A和E原子的最外层电子排布为ns1,则原子的最外层电子都只有一个电子,二者处于ⅠA族,结合原子序数可知,E为K元素、A为氢元素;
C元素原子的最外层电子数是S元素原子最外层电子数的一半,即C为Al,据此解答.
解答:
解:A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,B和D元素原子的最外层电子数相同,二者处于同主族,且它们原子最外层的p电子数是s电子数的两倍,则最外层含有6个电子,则B为氧元素、D为硫元素;
C、E是金属元素,A和E原子的最外层电子排布为ns1,则原子的最外层电子都只有一个电子,二者处于ⅠA族,结合原子序数可知,E为K元素、A为氢元素;
C元素原子的最外层电子数是S元素原子最外层电子数的一半,即C为Al,
(1)由上述分析可知,A为H,故答案为:H;
(2)C为Al元素,原子核外有13个电子,其电子排布式为:1s22s22p63s23p1,属于p区元素;
故答案为:1s22s22p63s23p1;p;
(3)Al形成的最高价氧化物的水化物为氢氧化铝,K的最高价氧化物的水化物是KOH,两者反应的离子反应方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)同主族从上到下,电负性逐渐减弱,则电负性:O>S;金属元素的原子越容易失去电子,则第一电离能越小,所以第一电离能:Al>K;
故答案为:O>S;Al>K;
(5)B为O元素,位于第二周期、第VIA主族,O原子有2个电子层,最外层有6个电子,原子结构示意图为: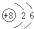 ;
;
故答案为:二、ⅥA;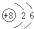 .
.
C、E是金属元素,A和E原子的最外层电子排布为ns1,则原子的最外层电子都只有一个电子,二者处于ⅠA族,结合原子序数可知,E为K元素、A为氢元素;
C元素原子的最外层电子数是S元素原子最外层电子数的一半,即C为Al,
(1)由上述分析可知,A为H,故答案为:H;
(2)C为Al元素,原子核外有13个电子,其电子排布式为:1s22s22p63s23p1,属于p区元素;
故答案为:1s22s22p63s23p1;p;
(3)Al形成的最高价氧化物的水化物为氢氧化铝,K的最高价氧化物的水化物是KOH,两者反应的离子反应方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)同主族从上到下,电负性逐渐减弱,则电负性:O>S;金属元素的原子越容易失去电子,则第一电离能越小,所以第一电离能:Al>K;
故答案为:O>S;Al>K;
(5)B为O元素,位于第二周期、第VIA主族,O原子有2个电子层,最外层有6个电子,原子结构示意图为:
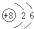 ;
;故答案为:二、ⅥA;
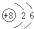 .
.
点评:本题考查结构性质位置关系,元素的推断是解答的关键,题目难度中等,注意掌握电子排布式的书写、离子方程式的书写、电负性、第一电离能等,旨在考查学生对基础知识的掌握.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
下列四组物质中,前者属于电解质,后者属于非电解质的是( )
| A、二氧化碳 碳酸钠 |
| B、硫酸钠 乙醇 |
| C、氧化铝 硫 |
| D、蔗糖 氢氧化钠 |
下列关于常见有机物的说法不正确的是( )
| A、乙烯和苯都能与溴水反应 |
| B、乙酸和油脂都能与氢氧化钠溶液反应 |
| C、糖类和蛋白质都是人体重要的营养物质 |
| D、乙烯和甲烷可用酸性高锰酸钾溶液鉴别 |
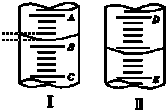 如图,图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,图Ⅱ表示50mL滴定管中液面的位置,D与E刻度间相差1mL.如果刻度A和D都是4,则两处液面的读数是( )
如图,图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,图Ⅱ表示50mL滴定管中液面的位置,D与E刻度间相差1mL.如果刻度A和D都是4,则两处液面的读数是( )| A、Ⅰ中是3.2mL,Ⅱ中是3.40mL |
| B、Ⅰ中是4.8mL,Ⅱ中是3.40mL |
| C、Ⅰ中是3.2mL,Ⅱ中是4.60mL |
| D、Ⅰ中是4.8mL,Ⅱ中是4.60mL |
可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
| A、将混合气体通过盛有硫酸的洗气瓶 |
| B、将混合气体通过盛有足量溴水的洗气瓶 |
| C、将混合气体通过盛有酸性KMnO4溶液的洗气瓶 |
| D、将混合气体通过盛有澄清石灰水的洗气瓶 |
在一定条件下发生下列反应,其中属于盐类水解反应的是( )
| A、NH4++2H2O?NH3?H2O+H3O+ |
| B、HCO3-+H2O?H3O++CO32- |
| C、Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ |
| D、CH3COOCH2CH3+H2O?CH3COOH+CH3CH2OH |
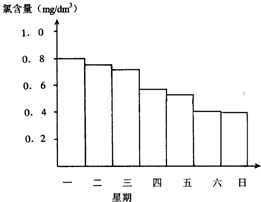 游泳池水的含氯气量应该控制在0.5mg/L至1.0mg/L之间,
游泳池水的含氯气量应该控制在0.5mg/L至1.0mg/L之间,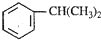 是一种重要的有机化工原料.根据题意完成下列
是一种重要的有机化工原料.根据题意完成下列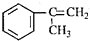 是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法
是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法