题目内容
15.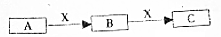 A、B、C是中学化学常见的三种物质.它们之间的相互转化关系如下(部分反条件及反应物产物略去)
A、B、C是中学化学常见的三种物质.它们之间的相互转化关系如下(部分反条件及反应物产物略去)(1)若X是CO2,A是NaOH溶液,在溶液中B→C的离子万程式为CO2+CO32-+H2O=2HCO3-;
(2)若X是金属铁,A是氯气,在溶液中检验B的阳离子的方法是加入KSCN;在C的溶液中加入氢氧化钠溶液,视察到的现象是:生成沉淀,迅速变为灰绿色,最后变成红褐色沉淀.发生变化的反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(3)若X是氧气,C是红棕色气体,则A化学式可能为NH3或N2,请写出C溶于水生成的稀溶液与铜反应的化学方程式:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,稀溶液中溶质所起作用是氧化剂和酸的作用.
分析 (1)若X是CO2,A是NaOH溶液,可知B为Na2CO3,C为NaHCO3;
(2)若X是金属铁,A是氯气,则B为FeCl3,C为FeCl2;
(3)若X是氧气,C是红棕色气体,应为NO2,则B为NO,A为NH3或N2.
解答 解:(1)若X是CO2,A是NaOH溶液,可知B为Na2CO3,C为NaHCO3,在溶液中B→C的离子万程式为CO2+CO32-+H2O=2HCO3-,
故答案为:CO2+CO32-+H2O=2HCO3-;
(2)若X是金属铁,A是氯气,则B为FeCl3,C为FeCl2,检验铁离子,可加入KSCN,溶液呈血红色,氯化亚铁加入氢氧化钠溶液,先生成白色絮状沉淀,迅速变为灰绿色,最终变为红褐色,反应的方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:加入KSCN;迅速变为灰绿色;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)若X是氧气,C是红棕色气体,应为NO2,则B为NO,A为NH3或N2,C溶于水生成的稀溶液为稀硝酸,具有强氧化性,可与铜反应,方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,反应中硝酸起到酸性和氧化剂的作用,
故答案为:NH3或N2;3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;氧化剂和酸的作用.
点评 本题考查无机物的推断,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握物质的性质以及转化关系,难度不大,学习中注意物质反应的现象.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列物质的俗称和结构简式相对应的是( )
| A. | 蚁酸CH3COOH | B. | 石炭酸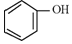 | C. | 氯仿CCl4 | D. | 甘油HOCH2CH2OH |
10.我国城市环境中的大气污染物主要是( )
| A. | SO2、NO2、CO、烟尘 | B. | HCl、SO2、N2、粉尘 | C. | NH3、CO2、NO、雾 | D. | CO2、Cl2、O2、酸雨 |
20.以下转化过程可以一步实现的是( )
| A. | SO2→H2SO4 | B. | SiO2→H2SiO3 | C. | Al2O3→Al(OH)3 | D. | Fe2O3→Fe(OH)3 |
7.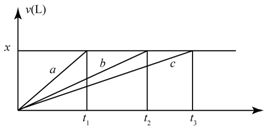 将等物质的量的金属Na、Mg、Al分别于100mL2mol•L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况),不正确的是( )
将等物质的量的金属Na、Mg、Al分别于100mL2mol•L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况),不正确的是( )
 将等物质的量的金属Na、Mg、Al分别于100mL2mol•L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况),不正确的是( )
将等物质的量的金属Na、Mg、Al分别于100mL2mol•L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况),不正确的是( )| A. | x=2.24 | B. | 钠的物质的量为0.2 mol | ||
| C. | 反应时,Na、Mg、Al均过量 | D. | 曲线b为Mg与盐酸反应的图象 |
4.钠、镁、铁、铜、硅、硫等元素中不能实现下列物质间直接转化有几种( )
单质→氧化物→酸或碱→盐.
单质→氧化物→酸或碱→盐.
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
19.在Al3++3H2O?Al(OH)3+3H+的平衡体系中,要使平衡向水解方向移动.且使溶液的pH增大,应采取的措施是( )
| A. | 加热 | B. | 通入HCl | ||
| C. | 加入适量的NaOH(固体) | D. | 加入固体NaCl |