题目内容
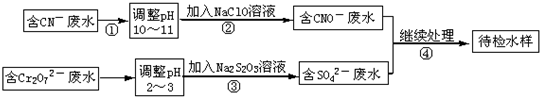
某工厂废渣含MgCO3、SiO2、Fe2O3、FeCO3和CaCO3、Al2O3.科研小组拟对废渣进行综合利用制取Mg(OH)2、芒硝(Na2SO4?10H2O)和Al2(SO4)3,设计如下工艺:

下表为几种沉淀的相关数据.回答以下问题:
(1)操作1名称是 ,该操作中所用到的玻璃仪器有 .
(2)你认为在除铁过程中选用下列物质中的 (填序号)作为试剂A是最合适的,
a.KMnO4 b.O2 c.H2O2 d.Cl2
并用离子方程式表示往滤液I中加入试剂A的目的 .现采用滴定的方法测定废渣中FeCO3的含量,取m克该工厂废渣加足量的H2SO4溶解后配成VmL溶液,从中取出10mL倒入锥形瓶中进行滴定,用一定浓度的试剂A进行滴定,则盛放试剂A的滴定管应选用 (填“酸式”或“碱式”),滴定终了时消耗浓度为c mol?L-1的试剂A共b mL,则该废渣中FeCO3的质量分数为 .
(3)滤液Ⅱ中加入试剂B目的是除Mg2+,根据溶度积可知pH=10.8时Mg2+已除尽,控制溶液pH=12.0的目的是 ,当pH=12.0时溶液中c(Mg2+)= .
(4)欲从滤液Ⅲ中分离出Al2(SO4)3溶液,依次加入的试剂可以是 . .

下表为几种沉淀的相关数据.回答以下问题:
| 物质名称 | 溶度积(Ksp) | pH | |
| 开始沉淀 | 完全沉淀 | ||
| Mg(OH)2 | 5.6×10-12 | 9.3 | 10.8 |
| Fe(OH)2 | 8.0×10-16 | 7.6 | 9.6 |
| Fe(OH)3 | 2.8×10-39 | 2.7 | 3.7 |
| Al(OH)3 | 1.3×10-33 | 3.7 | 4.7 |
(2)你认为在除铁过程中选用下列物质中的
a.KMnO4 b.O2 c.H2O2 d.Cl2
并用离子方程式表示往滤液I中加入试剂A的目的
(3)滤液Ⅱ中加入试剂B目的是除Mg2+,根据溶度积可知pH=10.8时Mg2+已除尽,控制溶液pH=12.0的目的是
(4)欲从滤液Ⅲ中分离出Al2(SO4)3溶液,依次加入的试剂可以是
考点:制备实验方案的设计
专题:实验设计题
分析:(1)工厂废渣含MgCO3、SiO2、Fe2O3、FeCO3和CaCO3、Al2O3,用硫酸溶解后得到可溶的硫酸镁、硫酸铁、硫酸亚铁、硫酸铝等物质和不溶的二氧化硅、硫酸钙,通过过滤除去不溶物得到滤液Ⅰ,根据过滤操作完成该操作所用到的玻璃仪器;
(2)从环境保护、氧化性、是否引进杂质方面考虑最佳试剂;双氧水将亚铁离子氧化成铁离子,据此写出反应的离子方程式;双氧水具有强氧化性,能够氧化碱式滴定管的橡胶管,所以应该使用酸式滴定管盛放;根据方程式计算出亚铁离子的物质的量,再计算出碳酸亚铁的质量分数;
(3)pH=12时使氢氧化铝完全溶解,从而得到更纯净的氢氧化镁;沉淀完全后的溶液中存在沉淀溶解平衡,依据氢氧化镁的溶度积常数计算出pH=12.0时溶液中c(Mg2+);
(4)滤液Ⅲ中含有偏铝酸根离子,偏铝酸根离子能够与二氧化碳反应生成氢氧化铝,过滤后得到氢氧化铝沉淀,然后加入稀硫酸获得硫酸铝.
(2)从环境保护、氧化性、是否引进杂质方面考虑最佳试剂;双氧水将亚铁离子氧化成铁离子,据此写出反应的离子方程式;双氧水具有强氧化性,能够氧化碱式滴定管的橡胶管,所以应该使用酸式滴定管盛放;根据方程式计算出亚铁离子的物质的量,再计算出碳酸亚铁的质量分数;
(3)pH=12时使氢氧化铝完全溶解,从而得到更纯净的氢氧化镁;沉淀完全后的溶液中存在沉淀溶解平衡,依据氢氧化镁的溶度积常数计算出pH=12.0时溶液中c(Mg2+);
(4)滤液Ⅲ中含有偏铝酸根离子,偏铝酸根离子能够与二氧化碳反应生成氢氧化铝,过滤后得到氢氧化铝沉淀,然后加入稀硫酸获得硫酸铝.
解答:
解:(1)根据题中流程可知,通过操作Ⅰ将不溶物和易溶物分离,通常使用过滤操作,过滤时需要使用的玻璃仪器有:烧杯、玻璃棒和漏斗,
故答案为:过滤;烧杯、玻璃棒、漏斗;
(2)根据表中溶度积可知,氢氧化亚铁完全沉淀时溶液的pH=9.6,与氢氧化镁完全沉淀的pH接近,不易直接除掉,需要用氧化剂氧化成铁离子,由于加入酸性高锰酸钾、氯水会引进杂质,氧气的氧化性较弱,氧化效果不好,所以最佳氧化剂为双氧水;
双氧水与亚铁离子反应的离子方程式为:2H++2Fe2++H2O2=2Fe3++2H2O;
滴定10mL样品的溶液时消耗的双氧水的物质的量为:cmol/L×b×10-3L=cb×10-3mol,根据反应2H++2Fe2++H2O2=2Fe3++2H2O可知,亚铁离子的物质的量为:n(Fe2+)=n(FeCO3)=2n(H2O2)=2cb×10-3mol,则VmL样品溶液中含有FeCO3的物质的量为:2cb×10-3mol×
=2cbV×10-4mol,所以该样品中含有FeCO3的质量分数为:
×100%=
%,
双氧水能够氧化碱式滴定管的橡胶管,所以应该用酸式滴定管盛放双氧水;
故答案为:c;2H++2Fe2++H2O2=2Fe3++2H2O;酸式;
%;
(3)pH=10.8时Mg2+已除尽,控制溶液pH=12.0目的是使生成的Al(OH)3尽可能的溶解,便于获得较纯净的Mg(OH)2沉淀;
已知Ksp[Mg(OH)2]=5.6×10-12,当控制溶液pH=12时,可确保Mg2+除尽,此时溶液中Mg2+的物质的量浓度为:c(OH-)=
mol/L=10-2mol/L,Ksp(Mg(OH)2)=c(Mg2+)×c2(OH-)=5.6×10-12,c(Mg2+)=
=5.6×10-8mol?L-1,
故答案为:使生成的Al(OH)3尽可能的溶解,便于获得较纯净的Mg(OH)2沉淀;5.6×10-8mol?L-1;
(4)滤液Ⅲ中铝元素以偏铝酸根离子形式存在,可以通入过量二氧化碳气体转化成氢氧化铝沉淀,然后在加入稀硫酸将氢氧化铝转化成硫酸铝,所以需要的试剂分别为:CO2、稀硫酸,
故答案为:CO2;稀硫酸.
故答案为:过滤;烧杯、玻璃棒、漏斗;
(2)根据表中溶度积可知,氢氧化亚铁完全沉淀时溶液的pH=9.6,与氢氧化镁完全沉淀的pH接近,不易直接除掉,需要用氧化剂氧化成铁离子,由于加入酸性高锰酸钾、氯水会引进杂质,氧气的氧化性较弱,氧化效果不好,所以最佳氧化剂为双氧水;
双氧水与亚铁离子反应的离子方程式为:2H++2Fe2++H2O2=2Fe3++2H2O;
滴定10mL样品的溶液时消耗的双氧水的物质的量为:cmol/L×b×10-3L=cb×10-3mol,根据反应2H++2Fe2++H2O2=2Fe3++2H2O可知,亚铁离子的物质的量为:n(Fe2+)=n(FeCO3)=2n(H2O2)=2cb×10-3mol,则VmL样品溶液中含有FeCO3的物质的量为:2cb×10-3mol×
| VmL |
| 10mL |
| 116g/mol×2cbV×10-3mol |
| mg |
| 23.2cbV |
| m |
双氧水能够氧化碱式滴定管的橡胶管,所以应该用酸式滴定管盛放双氧水;
故答案为:c;2H++2Fe2++H2O2=2Fe3++2H2O;酸式;
| 23.2cbV |
| m |
(3)pH=10.8时Mg2+已除尽,控制溶液pH=12.0目的是使生成的Al(OH)3尽可能的溶解,便于获得较纯净的Mg(OH)2沉淀;
已知Ksp[Mg(OH)2]=5.6×10-12,当控制溶液pH=12时,可确保Mg2+除尽,此时溶液中Mg2+的物质的量浓度为:c(OH-)=
| 10-14 |
| 10-12 |
| 5.6×10-12 |
| (10-2)2 |
故答案为:使生成的Al(OH)3尽可能的溶解,便于获得较纯净的Mg(OH)2沉淀;5.6×10-8mol?L-1;
(4)滤液Ⅲ中铝元素以偏铝酸根离子形式存在,可以通入过量二氧化碳气体转化成氢氧化铝沉淀,然后在加入稀硫酸将氢氧化铝转化成硫酸铝,所以需要的试剂分别为:CO2、稀硫酸,
故答案为:CO2;稀硫酸.
点评:本题通过Mg(OH)2、芒硝(Na2SO4?10H2O)和Al2(SO4)3的制备,考查了物质制备方案的设计,题目难度中等,涉及了化学基本实验操作方法、难溶物溶度积及其计算、物质的分离与提纯等知识,试题考查的知识点较多、综合性较强,有利于提高学生的分析、理解能力.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
下列离子的检验方法中正确的是( )
| A、某溶液加AgNO3溶液生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液加BaCl2溶液生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液加KOH溶液生成红褐色沉淀,说明原溶液中有Mg2+ |
 在如图所示的装置中,烧瓶中充满干燥的气体a,将滴管内的液体b挤入烧瓶内,轻轻振荡烧瓶,并打开弹簧夹,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别可能是( )
在如图所示的装置中,烧瓶中充满干燥的气体a,将滴管内的液体b挤入烧瓶内,轻轻振荡烧瓶,并打开弹簧夹,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别可能是( )| A、NO2和水 |
| B、SO2和NaOH溶液 |
| C、NH3和稀盐酸 |
| D、Cl2和饱和NaCl溶液 |
下列有关实验操作、现象或实验原理叙述错误的是( )
| A、纸层折法分离Fe3+和Cu2+的实验中,点样后的滤纸需晾干后可使用 |
| B、在中和热测定的实验中,可将反应前氢氧化钠溶液的温度作为起始温度 |
| C、将Kcl和NaNO3的混合液加热并浓缩至有晶体析出时,趁热过滤可分离得NaCl晶体 |
| D、(镀锌铁皮锌镀层厚度的测定)实验中,当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,借此可判断锌镀层是否反应完全 |
 如图装置,在关闭活塞K时通入气体X,b中溶液没有明显现象;开启活塞K通入气体X,则b中溶液有明显现象,下列判断中合理的是( )
如图装置,在关闭活塞K时通入气体X,b中溶液没有明显现象;开启活塞K通入气体X,则b中溶液有明显现象,下列判断中合理的是( )
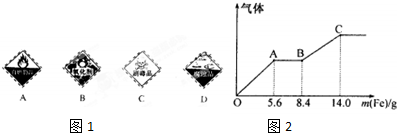 研究硫及其化合物的性质具有重要意义.
研究硫及其化合物的性质具有重要意义.