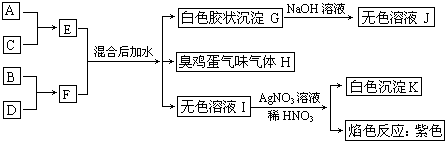
题目内容
下列叙述中正确的是( )
| A、不可用澄清石灰水鉴别Na2CO3和NaHCO3溶液 |
| B、1mol过氧化钠与2 mol碳酸钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是纯净物 |
| C、等质量的NaHCO3和Na2 CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D、可利用焰色反应来鉴别Na2CO3和NaHCO3固体 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:
分析:A、Na2CO3溶液和NaHCO3溶液均与石灰水反应生成白色沉淀;
B、过氧化钠与碳酸钠固体不反应,碳酸钠加热不易分解;
C、等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少;
D、Na2CO3和NaHCO3焰色反应都为黄色,不能鉴别.
B、过氧化钠与碳酸钠固体不反应,碳酸钠加热不易分解;
C、等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少;
D、Na2CO3和NaHCO3焰色反应都为黄色,不能鉴别.
解答:
解:A、澄清石灰水成分为Ca(OH)2,Na2CO3溶液和NaHCO3溶液均与Ca(OH)2反应生成白色沉淀CaCO3,现象相同,不能鉴别,故A正确;
B、过氧化钠与碳酸钠固体不反应,残留的固体物质是混合物,故B错误;
C、等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少,盐酸足量,则与盐酸完全反应,碳酸钠产生的气体少,故C错误;
D、Na2CO3和NaHCO3焰色反应都为黄色,不能鉴别,故D错误.
故选A.
B、过氧化钠与碳酸钠固体不反应,残留的固体物质是混合物,故B错误;
C、等质量的Na2CO3和NaHCO3,碳酸钠的摩尔质量大,其物质的量少,盐酸足量,则与盐酸完全反应,碳酸钠产生的气体少,故C错误;
D、Na2CO3和NaHCO3焰色反应都为黄色,不能鉴别,故D错误.
故选A.
点评:本题考查物质的检验,为高频考点,把握物质的性质及发生的反应、反应现象是解答本题的关键,注意物质性质的差异即可解答,题目难度不大.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列化合物中价键极性最小是( )
| A、MgCl2 |
| B、AlCl3 |
| C、SiCl4 |
| D、PCl5 |
某溶液中加入BaCl2溶液,生成不溶于稀盐酸的白色沉淀,则溶液中溶有的离子是( )
| A、一定溶有CO32- |
| B、一定溶有SO42- |
| C、一定溶有Ag+ |
| D、可能溶有SO42-或Ag+ |

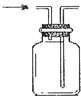


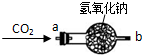 某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.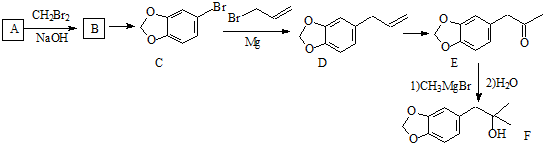
 系统命名为1-溴丙烯.
系统命名为1-溴丙烯.