题目内容
有关物质的量的计算填空.
(1)1.2gRSO4中含0.01molR2+,则R的摩尔质量是 ;
(2)多少摩尔H2SO4与1.806×1024个水分子含有相同的氧原子数.
(3)Na2SO4和Al2(SO4)3 的混合溶液中,SO42-的物质的量浓度为1mol/L,Na+的物质的量浓度为0.8mol/L,则Al3+的物质的量浓度为 mol/L.
(1)1.2gRSO4中含0.01molR2+,则R的摩尔质量是
(2)多少摩尔H2SO4与1.806×1024个水分子含有相同的氧原子数.
(3)Na2SO4和Al2(SO4)3 的混合溶液中,SO42-的物质的量浓度为1mol/L,Na+的物质的量浓度为0.8mol/L,则Al3+的物质的量浓度为
考点:物质的量的相关计算
专题:计算题
分析:(1)由化学式可知n(RSO4)=n(R2+),根据M=
计算RSO4的摩尔质量,进而计算R的摩尔质量;
(2)根据n=
计算水的物质的量,根据氧原子计算硫酸的物质的量;
(3)溶液呈电中性,根据电荷守恒,溶液中2c(SO42-)=c(Na+)+3c(Al3+),据此计算解答.
| m |
| M |
(2)根据n=
| N |
| NA |
(3)溶液呈电中性,根据电荷守恒,溶液中2c(SO42-)=c(Na+)+3c(Al3+),据此计算解答.
解答:
解:(1)由化学式可知n(RSO4)=n(R2+)=0.01mol,则RSO4的摩尔质量为
=120g/mol,故R的摩尔质量为120g/mol-96g/mol=24g/mol,
故答案为:24g/mol;
(2)水的物质的量为
=0.3mol,与之含有相同氧原子数目的硫酸的物质的量为
=0.075mol,
答:硫酸的物质的量为0.075mol;
(3)溶液呈电中性,根据电荷守恒,溶液中2c(SO42-)=c(Na+)+3c(Al3+),即2×1mol/L=0.8mol/L+3c(Al3+),解得c(Al3+)=0.4mol/L,
故答案为:0.4.
| 1.2g |
| 0.01mol |
故答案为:24g/mol;
(2)水的物质的量为
| 1.806×1023 |
| 6.02×1023mol-1 |
| 0.3mol |
| 4 |
答:硫酸的物质的量为0.075mol;
(3)溶液呈电中性,根据电荷守恒,溶液中2c(SO42-)=c(Na+)+3c(Al3+),即2×1mol/L=0.8mol/L+3c(Al3+),解得c(Al3+)=0.4mol/L,
故答案为:0.4.
点评:本题考查物质的量有关计算,难度不大,注意电解混合溶液中常利用电荷守恒计算离子的浓度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
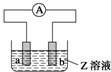 如图中a、b分别是原电池的两极,接通电路后发现a极板质量增加,b极板溶解,
如图中a、b分别是原电池的两极,接通电路后发现a极板质量增加,b极板溶解,符合这一情况的是( )
| a极板 | b极板 | a电极 | Z溶液 | |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 正极 | AgNO3 |
| D | 铜 | 石墨 | 正极 | CuCl2 |
| A、A | B、B | C、C | D、D |
45mL某气体,可能含有CO2、O2、NH3将其通过浓硫酸,气体体积无变化,通过足量的Na2O2后,体积变为30mL,则该气体的组成为( )
| A、CO2为30mL,O2为15mL |
| B、NH3为30mL,O2为15mL |
| C、CO2为15mL,O2为30mL |
| D、CO2 为30mL,O2为15mL |
下列离子方程式书写正确的是( )
| A、FeO固体放入稀硝酸溶液中:FeO+2H+═Fe2++H2O |
| B、过量的铁粉与稀硝酸溶液反应:Fe+4H++NO3-═Fe3++NO↑+2H2O |
| C、向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
| D、向Fe(OH)3中加入氢碘酸:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O |
两个容积相同的容器中,一个盛有CO 气体,另一个盛有N2气.在同温同压下,两容器内的气体一定具有相同的:①分子数 ②原子数 ③质量 ④质子数 ⑤电子数( )
| A、只有①② | B、只有①②③ |
| C、只有①②④ | D、全部 |
下列关于电解质溶液的叙述中正确的是( )
| A、Na2CO3、NaHCO3两种盐的溶液中,离子种类相同 | ||
| B、在CH3COONa溶液中c (CH3COO-)>c(Na+)>c(OH-)>c(H+) | ||
C、在0.1mol?L-1的醋酸溶液中加入适量的蒸馏水,溶液的
| ||
| D、常温下,某溶液中由水电离出的c(H+)为10-5 mol/L,则此溶液可能是盐酸 |
下列化学反应对应的离子方程式正确的是( )
| A、KOH溶液与KHSO4溶液反应:OH-+H+═H2O |
| B、稀H2SO4与Ba(OH)2溶液反应:H++SO42-+OH-+Ba2+═BaSO4↓+H2O |
| C、铁与盐酸反应:Fe+2H+═Fe3++H2↑ |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
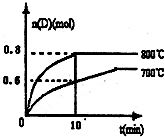 (1)已知:N2(g)+O2(g)=2NO(g)△H=180.5kJ?mol-1
(1)已知:N2(g)+O2(g)=2NO(g)△H=180.5kJ?mol-1