题目内容
下列说法不正确的是( )
| A、二氧化硅是制造光导纤维的材料,单质硅是良好的半导体材料 |
| B、SiO2和CO2都是酸性氧化物,但SiO2不能和水反应生成硅酸 |
| C、保存NaOH溶液时不能用玻璃塞 |
| D、二氧化硅性质稳定,不与任何酸反应 |
考点:硅和二氧化硅
专题:碳族元素
分析:A、依据二氧化硅和硅单质性质分析判断;
B、和碱反应生成盐和 水的氧化物为酸性氧化物,二氧化硅不溶于水;
C、氢氧化钠溶液和玻璃中的二氧化硅反应生成的硅酸钠溶液是矿物胶,能粘结瓶口和瓶塞;
D、二氧化硅和氢氟酸反应;
B、和碱反应生成盐和 水的氧化物为酸性氧化物,二氧化硅不溶于水;
C、氢氧化钠溶液和玻璃中的二氧化硅反应生成的硅酸钠溶液是矿物胶,能粘结瓶口和瓶塞;
D、二氧化硅和氢氟酸反应;
解答:
解:A、依据二氧化硅和硅单质性质分析判断,二氧化硅是制造光导纤维的材料,单质硅是良好的半导体材料,故A正确;
B、和碱反应生成盐和水的氧化物为酸性氧化物,SiO2和CO2都是酸性氧化物,二氧化硅不溶于水,不能溶于水生成硅酸,故B正确;
C、氢氧化钠溶液和玻璃中的二氧化硅反应生成的硅酸钠溶液是矿物胶,能粘结瓶口和瓶塞,保存NaOH溶液时不能用玻璃塞,故C正确;
D、二氧化硅和氢氟酸反应,故D错误;
故选D.
B、和碱反应生成盐和水的氧化物为酸性氧化物,SiO2和CO2都是酸性氧化物,二氧化硅不溶于水,不能溶于水生成硅酸,故B正确;
C、氢氧化钠溶液和玻璃中的二氧化硅反应生成的硅酸钠溶液是矿物胶,能粘结瓶口和瓶塞,保存NaOH溶液时不能用玻璃塞,故C正确;
D、二氧化硅和氢氟酸反应,故D错误;
故选D.
点评:本题考查了硅、二氧化硅性质的 分析应用,掌握物质分类和特征性质是解题关键,题目较简单.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
下列说法正确的是( )
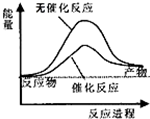

| A、如图可表示水分解过程中的能量变化 |
| B、高温高压下的超临界水,溶液中的氢离子和氢氧根离子浓度较大,有时显酸性,有时显碱性 |
| C、需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D、等体积、等浓度的醋酸钠溶液和次氯酸钠溶液中,所含离子总数,前者小于后者 |
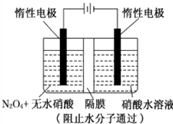 如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )
如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )| A、阴极的电极反应为:NO3-+4H++3e-=NO↑+2H2O |
| B、阳极的电极反应为:N2O4+2 HNO3-2e-=2N2O5+2H+ |
| C、当电路中通过6 mol e-时整个电解池中参与反应的HNO3为8mol |
| D、当电路中通过6 mol e-时,有8molH+从阳极向阴极迁移 |
下列说法正确的是( )
| A、凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B、自发反应在恰当条件下才能实现 |
| C、自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| D、自发反应在任何条件下都能实现 |
检验某液态卤代烃中是否含氯元素,正确的实验方法是( )
| A、加入溴水振荡,观察水层是否有棕红色出现 |
| B、滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无白色沉淀生成 |
| C、加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无白色沉淀生成 |
| D、加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无白色沉淀生成 |
生活中常见的三种物质:①柠檬汁,②肥皂水,③食盐水,按溶液pH由小到大排列正确的是( )
| A、①②③ | B、.①③② |
| C、.③②① | D、.②①③ |
下列说法正确的是( )
| A、酸、碱和盐类都属于电解质,其他化合物都是非电解质 |
| B、强电解质与弱电解质的本质区别,是其水溶液导电性的减弱 |
| C、电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 |
| D、常见的强酸、强碱和大部分盐都是强电解质,其他化合 物都是非电解质 |
下列有关物质分类或归类错误的是( )
| A、混合物:盐酸、生铁、空气 |
| B、化合物:CaCl2、NaOH、HCl |
| C、盐:CaO、BaSO4、NaCl |
| D、单质:Ca、O3、石墨 |
按下列路线制聚氯乙烯,不发生的反应类型是( )
C2H5Br
CH2=CH2
CH2Cl
CH2ClCH2=CHCl

C2H5Br
| ① |
| ② |
| ③ |
| ④ |

| A、加成反应 | B、消去反应 |
| C、取代反应 | D、加聚反应 |