题目内容
15.下列有关关仪器的使用方法或实验操作正确的是( )| A. | 配制一定物质的量浓度溶液中,洗净的容量瓶要放进烘箱中烘干,以防溶液被稀释 | |
| B. | 测量Zn与稀硫酸反应速率的实验中,应在标准状况下测量H2的体积,以方便计算 | |
| C. | 酸碱滴定实验中,用待测溶液润洗锥形瓶,以减少实验误差 | |
| D. | 中和热的测定实验中,要用环形玻璃搅拌棒搅拌,使反应更充分 |
分析 A.容量瓶不需要烘干;
B.测定速率,需要测定时间与气体体积变化;
C.酸碱滴定实验中,锥形瓶不需要润洗;
D.中和热的测定实验中,要用环形玻璃搅拌棒搅拌,测定最高温度.
解答 解:A.容量瓶不需要烘干,有少量水对实验无影响,最后需要加水定容,故A错误;
B.测定速率,需要测定时间与气体体积变化,不需要控制标准状况下,故B错误;
C.酸碱滴定实验中,锥形瓶不需要润洗,若用待测溶液润洗锥形瓶,测定结果偏大,故C错误;
D.中和热的测定实验中,要用环形玻璃搅拌棒搅拌,使反应更充分,测定最高温度,操作合理,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液配制、中和滴定、中和热测定为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.下列有机物中,互为同分异构体的是( )
| A. | 葡萄糖和果糖 | B. | 淀粉和纤维素 | ||
| C. | 硬脂酸和软脂酸 | D. | 甘氨酸和硝基乙烷 |
6.室温下,将1.000mol•L-1盐酸逐滴滴入20.00mL 1.000mol•L-1氨水中.溶液的pH和温度随加入盐酸的体积变化曲线如图所示.下列说法不正确的是( )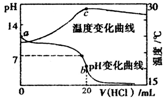

| A. | a点由水电离出的c(H+)<1.0×10-14mol•L-1 | |
| B. | b点时存在c(NH4+)+c(NH3•H2O)=c(C1-) | |
| C. | c点以后溶液温度下降的原因是盐酸的持续加入 | |
| D. | 在整个过程中可能会出现的离子浓度关系:c(NH4+)=c(C1-)>c(H+)=c(OH-) |
3.以黄铜矿(主要成分二硫化亚铁铜CuFeS2)为原料,用Fe2(SO4)3溶液作浸取剂提取铜,总反应的离子方程式是CuFeS2+4Fe3+?Cu2++5Fe2++2S.
(1)该反应中,Fe3+体现氧化性.
(2)上述总反应的原理如图1所示.负极的电极反应式是CuFeS2-4e-═Fe2++2S+Cu2+.
(3)一定温度下,控制浸取剂pH=1,取三份相同质量黄铜矿粉末分别进行如下实验:
①对比实验 I、II,通入空气,Cu2+浸出率提高的原因是通入O2后,发生反应4Fe2++O2+4H+═4Fe3++2H2O,c(Fe2+)降低,c(Fe3+)升高,总反应的平衡正向移动.
②由实验 III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+═Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+═2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005mol•L-1 Ag2SO4溶液,充分混合后静置.取上层清液,加入稀盐酸,观察到溶液中无明显现象,证明发生反应 i.
b.取少量Ag2S粉末,加入pH=1的0.10mol•L-1Fe2(SO4)3溶液溶液,充分混合后静置.取上层清液,加入稀盐酸,有白色沉淀,证明发生反应 ii.
(4)用实验 II的浸取液电解提取铜的原理如图2所示:
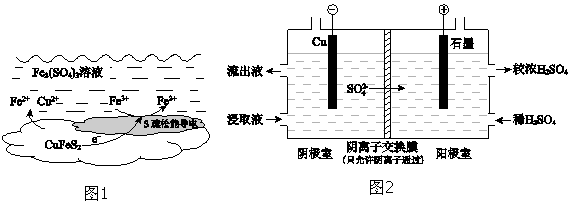
①电解初期,阴极没有铜析出.用电极反应式解释原因是Fe3++e-═Fe2+.
②将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是Fe2+在阳极失电子生成Fe3+:Fe2+-e-═Fe3+,SO42-通过阴离子交换膜进入阳极室,Fe2(SO4)3溶液再生.
(1)该反应中,Fe3+体现氧化性.
(2)上述总反应的原理如图1所示.负极的电极反应式是CuFeS2-4e-═Fe2++2S+Cu2+.
(3)一定温度下,控制浸取剂pH=1,取三份相同质量黄铜矿粉末分别进行如下实验:
| 实验 | 操作 | 2小时后Cu2+浸出率/% |
| I | 加入足量0.10mol•L-1 Fe2(SO4)3溶液 | 78.2 |
| II | 加入足量0.10mol•L-1 Fe2(SO4)3溶液,通入空气 | 90.8 |
| III | 加入足量0.10mol•L-1 Fe2(SO4)3溶液,再加入少量0.0005mol•L-1 Ag2SO4溶液 | 98.0 |
②由实验 III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+═Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+═2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005mol•L-1 Ag2SO4溶液,充分混合后静置.取上层清液,加入稀盐酸,观察到溶液中无明显现象,证明发生反应 i.
b.取少量Ag2S粉末,加入pH=1的0.10mol•L-1Fe2(SO4)3溶液溶液,充分混合后静置.取上层清液,加入稀盐酸,有白色沉淀,证明发生反应 ii.
(4)用实验 II的浸取液电解提取铜的原理如图2所示:

①电解初期,阴极没有铜析出.用电极反应式解释原因是Fe3++e-═Fe2+.
②将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是Fe2+在阳极失电子生成Fe3+:Fe2+-e-═Fe3+,SO42-通过阴离子交换膜进入阳极室,Fe2(SO4)3溶液再生.
10.化学与社会、生产、生活和科技都密切相关.下列说法正确的是( )
| A. | 军舰船底镶嵌锌块作正极,以防船体被腐蚀 | |
| B. | “天宫二号”使用的碳纤维,是一种新型有机高分子材料 | |
| C. | 烈性炸药硝化甘油是由甘油(丙三醇)硝化制得,它属于酯类 | |
| D. | 蚊虫叮咬时释放出的蚁酸使人觉得不适,可以用肥皂水氧化蚁酸处理 |
20.25℃时,向10mL0.1mol/L H2A溶液中滴加等浓度的NaOH溶液,混合后溶液的pH 与所加NaOH 溶液的体积关系如图所示.下列叙述正确的是( )

| A. | NaHA的电离方程式为NaHA?Na++HA- | B. | B点:c(H2A)+c(H+)=c(OH-)+c(A2-) | ||
| C. | C点:c(Na+)=c(A2-)+c(HA-) | D. | D点:c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+) |
7.amolFeS与bmolFeO投入VLcmol/L的HNO3溶液(过量)中,充分反应,产生气体为NO,则反应后溶液中NO3-的量为( )
| A. | 62(a+b)g | B. | 186(a+b)g | C. | (cV-$\frac{a+b}{3}$)mol | D. | (cV-$\frac{9a+b}{3}$)mol |
4.14C 常用于测定年代,关于其说法正确的是( )
| A. | 比 12C 多两个质子 | B. | 与 12C 化学性质相似 | ||
| C. | 与 12C 互为同素异形体 | D. | 质子数与中子数相等 |
6.下列说法不正确的是( )
| A. | 0.02 mol•L-1醋酸与0.02 mol•L-1NaOH等体积混合后的溶液中加少量的CH3COONa固体,则$\frac{c(C{H}_{3}CO{O}^{-})}{C(N{a}^{+})}$ 增大 | |
| B. | t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2,$\frac{c(NO)•c(S{O}_{3})}{c(N{O}_{2})•c(S{O}_{2})}$ 的值及SO2转化率不变 | |
| C. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 | |
| D. | lmol该化合物( 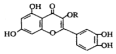 )与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4mol、8mol )与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4mol、8mol |