题目内容
6.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm).| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
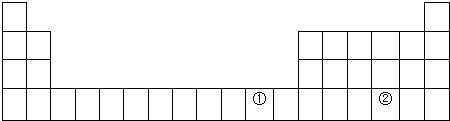
(2)①元素处于元素周期表中四周期IB族;写出该元素(Cu)单质在空气中生锈的方程式2Cu+O2+CO2+H2O=Cu2(OH)2CO3;
(3)A的离子结构示意图为
 .B的氧化物溶于氢氧化钠溶液的方程式为Al2O3+2NaOH+3=2NaAlO2+H2O;
.B的氧化物溶于氢氧化钠溶液的方程式为Al2O3+2NaOH+3=2NaAlO2+H2O;(4)用一个化学方程式证明C、D元素非金属性强弱Cl2+H2S=S↓+2HCl;
(5)元素②与C的最高价含氧酸酸性由强到弱顺序为H2SO4>H2SeO4.(用化学式表示)
分析 C、E都有-2价,处于ⅥA族,且C有+6价、原子半径较大,故C为S元素、E为O元素;A有+2价,处于ⅡA族,且原子半径A>硫,故A为Mg;B有+3价,原子半径大于S,故B为Al元素;F有-1价,原子半径大于氧原子的,则F为Cl.
(1)主族元素周期数=电子层数、主族族序数=最外层电子数;
(2)由元素位置可知,①处于周期表中第四周期IB族;在空气中Cu与氧气、水、二氧化碳反应生成碱式碳酸铜;
(3)A的离子为Mg2+,离子核外有10个电子,各层电子数为2、8;B的氧化物为氧化铝,与氢氧化钠溶液反应生成偏铝酸钠与水;
(4)A利用元素单质之间相互置换反应可以证明元素非金属性强弱;
(5)元素的非金属性越强,最高价含氧酸的酸性越强.
解答 解:C、E都有-2价,处于ⅥA族,且C有+6价、原子半径较大,故C为S元素、E为O元素;A有+2价,处于ⅡA族,且原子半径A>硫,故A为Mg;B有+3价,原子半径大于S,故B为Al元素;F有-1价,原子半径大于氧原子的,则F为Cl.
(1)Mg元素位于第三周期第IIA族、Al元素位于第三周期第IIIA族、S位于第三周期第VIA族、Cl元素位于第三周期第VIIA、O元素位于第二周期第VIA族,在元素周期表中位置为: ,
,
故答案为: ;
;
(2)由元素位置可知,①处于周期表中第四周期IB族;在空气中Cu与氧气、水、二氧化碳反应生成碱式碳酸铜,反应方程式为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3,
故答案为:四、IB;2Cu+O2+CO2+H2O=Cu2(OH)2CO3;
(3)A的离子为Mg2+,离子核外有10个电子,各层电子数为2、8,离子结构示意图为 ;B的氧化物为氧化铝,与氢氧化钠溶液反应生成偏铝酸钠与水,反应方程式为:Al2O3+2NaOH+3=2NaAlO2+H2O,
;B的氧化物为氧化铝,与氢氧化钠溶液反应生成偏铝酸钠与水,反应方程式为:Al2O3+2NaOH+3=2NaAlO2+H2O,
故答案为: ;Al2O3+2NaOH+3=2NaAlO2+H2O;
;Al2O3+2NaOH+3=2NaAlO2+H2O;
(4)A利用元素单质之间相互置换反应可以证明元素非金属性强弱,反应方程式为:Cl2+H2S=S↓+2HCl,
故答案为:Cl2+H2S=S↓+2HCl;
(5)非金属性S>Se,元素的非金属性越强,最高价含氧酸的酸性越强,故酸性:H2SO4>H2SeO4,
故答案为:H2SO4>H2SeO4.
点评 本题考查结构性质位置关系应用,根据化合价与原子半径推断元素是解题关键,注意元素周期律的理解掌握,难度不大.

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案| A. | M元素一定是第VA族元素 | |
| B. | M元素一定是第三周期元素 | |
| C. | M可形成与CH3CHO电子数相等的化合物 | |
| D. | M的单质在空气中加热时可能会生成红棕色气体 |
| A. | C2H5Br | B. | 氯水 | C. | 溴的CCl4溶液 | D. | KClO3溶液 |
| W | X | Y | |
| Z |
(1)Y在元素周期表的位置是第三周期第ⅥA族,其氢化物的电子式为
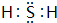 .
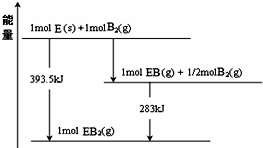
.(2)B元素与Y、Z同主族,且原子半径比二者小.E是形成化合物种类最多的元素,已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图所示,请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5 kJ•mol -1.
(3)25℃时,NaH2XO2溶液pH>7,向100mL 0.01mol•L-1的H3XO2溶液中,滴加等浓度的NaOH溶液至溶液呈中性,消耗NaOH溶液的体积<(填“>”、“=”或“<”)100mL.
(4)W的最高价氧化物能溶于烧碱溶液,该反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O.现取100mL 1mol•L-1W的氯化物溶液,向其中加入1mol•L-1NaOH溶液产生了3.9g的沉淀,则加入的氢氧化钠溶液体积可能是150或350 mL.
(5)探究同主族元素性质的相似性,是学习化学的重要方法之一.在下表中列出对H2ZO3各种不同化学性质的推测,请根据示例填写下列空格(Z元素符号仍用Z表示)
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2ZO3+4HI═Z↓+2I2+3H2O |
| ① | 还原性 | |
| ② | H2ZO3+2NaOH═Na2ZO3+2H2O |
| A. | 丙烯 | B. | 乙烯 | C. | 苯 | D. | 酒精 |
| A. | 砹是一种有色固体,它的气态氢化物很不稳定 | |
| B. | F2与水反应比Cl2与水反应剧烈 | |
| C. | 铷的最高价氧化物的水化物一定是强碱 | |
| D. | 由Cl元素和S元素的最低化合价分别为-1和-2,推知元素的非金属性S>Cl |
| A. |  加热NaHCO3固体 | B. |  中和滴定 | ||
| C. |  用苯萃取碘水分离苯层的操作 | D. |  除去氨气中的水蒸气 |