题目内容
4.对于下列有机物异构体数目的判断错误的是(不考虑空间异构)( )| A. | 分子式为C6H14含有四个甲基的烃的一氯取代物的异构体数目为5 | |
| B. | 分子式为C5H10异构体数目为5 | |
| C. | 分子式为C4H10O的醇类异构体数目为4 | |
| D. | 分子式为C6H12O2羧酸类异构体数目为8 |
分析 A.C6H14属于烷烃,根据甲基数目写出符合条件的同分异构体的结构简式,利用等效氢判断其一氯代物的数目;
B.组成为C5H10的有机物,其所有同分异构体中有烯烃,同分异构体说明含有1个C=C双键,根据碳链缩短法书写同分异构体;
C.分子式为C4H10O的物质是醇类有机化合物,同分异构体有4种;
D.分子式为C6H12O2且含有羧基的有机物可以简写为C5H11COOH,其中-C5H11有8种同分异构体.
解答 解:A.含4个甲基,则有 和
和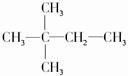 两种结构,前一种有2种一氯代物,后一种有3种一氯代物,故A错误;
两种结构,前一种有2种一氯代物,后一种有3种一氯代物,故A错误;
B.戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、 、
、 .
.
若为CH3-CH2-CH2-CH2-CH3,相应烯烃有CH2═CH-CH2-CH2-CH3、CH3-CH═CH-CH2-CH3,即有2种异构.
若为 ,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2,都不存在顺反异构,即有3种异构.
,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2,都不存在顺反异构,即有3种异构.
若为 ,没有相应烯烃.
,没有相应烯烃.
所以分子式为C5H10的烯烃共有(不包括顺反异构)2+3=5种,故B正确;
C.分子式为C4H10O,是醇类有机化合物的同分异构体,有4种,即: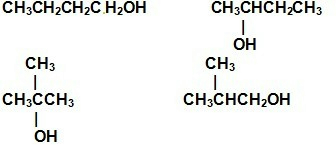 ,故C正确;
,故C正确;
D.分子式为C6H12O2且含有羧基的有机物可以简写为C5H11COOH,其中-C5H11有8种同分异构体:CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,所以C5H11COOH有8种同分异构体,故D正确.
故选A.
点评 本题考查同分异构体的书写,难度不大,根据甲基数目书写符合条件的同分异构体结构是关键.

| A. | HCl分子的电子式H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{Cl}}{••}$${\;}_{•}^{•}$]- | |
| B. | 乙炔分子的结构式CH≡CH | |
| C. | H2O分子的比例模型 | |
| D. | 甲烷分子的球棍模型 |
| A. | 10ml | B. | 30ml | C. | 50ml | D. | 70ml |
| A. | NaCl溶液 | B. | NaOH溶液 | C. | NaHSO3溶液 | D. | NaHSO4溶液 |
(1)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据表信息,结合工业生产实际,选择最合适的生产条件是400℃,1个标准大气压.
| 压强 SO2转化率 温度 | 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
A.保持温度和容器体积不变,充入1mol O2(g)
B.保持温度和容器体积不变,充入2mol SO3 (g)
C.降低温度
D.在其他条件不变时,减小容器的容积.
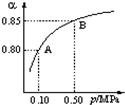
(3)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示,2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa.平衡状态由A编导B时,平衡常数K(A)=K(B)(填“<”,“>”,或“=”),B点的化学平衡常数是800.
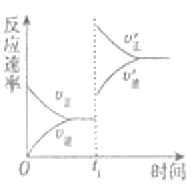
 (4)在一个固定容器为5L的密闭容器中充入0.20mol SO2(g)和0.10mol O2(g),t1时刻达到平衡,测得容器中含SO30.18mol.①t1时刻达到平衡后,改变一个条件使化学反应速度发生如图所示的变化,则改变的条件是C.
(4)在一个固定容器为5L的密闭容器中充入0.20mol SO2(g)和0.10mol O2(g),t1时刻达到平衡,测得容器中含SO30.18mol.①t1时刻达到平衡后,改变一个条件使化学反应速度发生如图所示的变化,则改变的条件是C.A.体积不变,向容器中通入少量O2
B.体积不变,向容器中通入少量SO2
C.缩小容器体积
D.升高温度
E.体积不变,向容器中通入少量氮气
②若继续通入0.20mol SO2和0.10mol O2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36 mol<n(SO3)<0.40mol.