题目内容
19.下列说法中正确的是( )| A. | 乙烯和苯都能使溴水褪色,且褪色原因相同 | |
| B. | 苯和四氯化碳都是无色液体,都难溶于水,所以用蒸馏水无法鉴别苯和四氯化碳 | |
| C. | 用氢氧化铜悬浊液不能区别甲酸和乙酸 | |
| D. | 乙醇、乙酸乙酯、乙酸能用饱和碳酸钠溶液鉴别 |
分析 A.苯和溴水不反应,发生萃取,溶液分层;
B.苯和四氯化碳的密度不同;
C.甲酸具有酸性和还原性,乙酸具有酸性;
D.乙醇溶于水,乙酸与碳酸钠反应,乙酸乙酯不溶于饱和碳酸钠溶液.
解答 解:A.乙烯与溴水发生加成反应,苯和溴水不反应,发生萃取,溶液分层,原理不同,故A错误;
B.苯和四氯化碳的密度不同,苯的密度比水小,四氯化碳的密度比水大,可鉴别,故B错误;
C.甲酸具有酸性和还原性,乙酸具有酸性,甲酸在加热条件下可与氢氧化铜发生氧化还原反应,现象不同,可鉴别,故C错误;
D.乙醇溶于水,乙酸与碳酸钠反应,乙酸乙酯不溶于饱和碳酸钠溶液,可鉴别,故D正确.
故选D.
点评 本题综合考查有机物的鉴别,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的性质的异同,难道不大,注意相关基础知识的积累.

练习册系列答案
相关题目
9.下列物质的水溶液不具有漂白性的是( )
| A. | Cl2 | B. | Ca(ClO)2 | C. | HClO | D. | HCl |
10.为了除去蛋白质溶液中混入的少量氯化钠,可以采用的方法是( )
| A. | 过滤 | B. | 盐析 | ||
| C. | 渗析 | D. | 加入AgNO3溶液,过滤 |
7.从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
| A. | 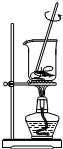 将海带灼烧成灰 | B. | 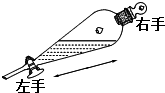 萃取振摇 | ||
| C. | 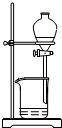 放出碘的苯溶液 | D. | 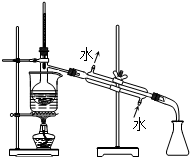 分离碘并回收苯 |
14.如图所示是部分短周期元素主要化合价与原子序数的关系图,下列说法不正确的是( )

| A. | X和W位于同一主族 | |
| B. | 原子半径:Y>Z>X | |
| C. | 盐YRX与化合物WX2的漂白原理相同 | |
| D. | Y和R两者的最高价氧化物对应的水化物能相互反应 |
11.下列说法错误的是( )
| A. | 过渡元素全是d区元素 | B. | 非金属元素大多数在p区 | ||
| C. | 过渡元素全是金属元素 | D. | s区元素包括ⅠA族和ⅡA族元素 |
8.室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中$\frac{{c(C{H_3}CO{O^-})}}{{c(C{H_3}COOH)•c(O{H^-})}}$不变 | |
| C. | 醋酸的电离程度增大,溶液酸性增强 | |
| D. | 再加入10mL pH=11的NaOH溶液,混合液pH=7 |
11.下列热化学方程式或叙述正确的是( )
| A. | 1 mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642kJ的热量:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=+642 kJ•mol-1 | |
| B. | 12 g石墨转化为CO时,放出110.5 kJ的热量:2C(石墨,s)+O2(g)═2CO(g)△H=-110.5 kJ•mol-1 | |
| C. | 已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286 kJ•mol-1,则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJ•mol-1 | |
| D. | 已知N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol-1,则在一定条件下向密闭容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反应放出46.2 kJ的热量 |
 .
.