题目内容
20.在由氧化铜和氧化铁组成的a g混合物中,取其一半加入2mol•L-1的稀盐酸溶液50mL,固体恰好完全溶解;若将原混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为( )| A. | 1.6a g | B. | (a-1.6)g | C. | (a-3.2)g | D. | (2a-3.2)g |
分析 氧化铜和氧化铁的混合物与与水反应生成氯化物与水,由于HCl中H元素与混合物中O元素结合生成水,则$\frac{1}{2}$ag 混合物中n(O)=$\frac{1}{2}$n(HCl),根据m=nM计算混合物中O元素质量,将ag这种混合物在CO流中加热并充分反应,冷却后剩余固体为Fe、Cu,金属质量等于氧化物质量减去氧元素质量.
解答 解:氧化铜和氧化铁的混合物与与水反应生成氯化物与水,由于HCl中H元素与混合物中O元素结合生成水,则$\frac{1}{2}$ag 混合物中n(O)=$\frac{1}{2}$n(HCl)=$\frac{1}{2}$×0.05L×2mol/L=0.05mol,则混合物中n(O)=2×0.05mol=0.1mol,故ag该混合物中O元素质量为:0.1mol×16g/mol=1.6g,若将ag这种混合物在CO流中加热并充分反应,冷却后剩余固体为Fe、Cu,则固体质量为ag-1.6g=(a-1.6)g,故选B.
点评 本题考查混合物的计算,难度中等,关键是根据HCl中H元素与混合物中O元素结合生成水确定混合物中氧元素物质的量.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
10.某温度下,CuSO4饱和溶液的质量分数为a%,取一定量的此饱和溶液,向其中加入m g无水CuSO4,在温度不变的情况下析出W g CuSO4•5H2O晶体,则原饱和溶液中溶质CuSO4的质量减少( )
| A. | m×a% | B. | W×a% | C. | (m+W)×a% | D. | (W-m)×a% |
11.下列离子组能够大量共存的是( )
| A. | 无色溶液中:Cu2+、K+、NO3-、Cl- | |
| B. | 使pH试纸显红色的溶液中:Fe2+、K+、NO3-、Cl- | |
| C. | 含MnO4-的溶液中:Fe3+、SO42-、NO3-、Mg2+ | |
| D. | 与铝作用生成氢气的溶液中:Mg2+、NO3-、K+、Cl- |
8.下列离子方程式书写正确的是( )
| A. | 在100ml 1mol•L-1的Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | 在100ml 2mol•L-1的FeI2的溶液中通入标况下5.6L的Cl2:4Fe2++6I-+5Cl2═4Fe3++3I2+10Cl- | |
| C. | 向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | AlCl3溶液中加入过量的NaOH溶液:Al3++4OH-═AlO2-+2H2O |
15.如图所示为电化学降解NO3-.下列说法中正确的是( )


| A. | 铅蓄电池的A极为阴极 | |
| B. | 电解的过程中有H+从右池移动到左池 | |
| C. | 该电解池的阴极反应为:2NO3-+6H2O+12e-=N2↑+12OH- | |
| D. | 若电解过程中转移1moL电子,则交换膜两侧电解液的质量变化差为7.2g |
5.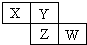 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐 | |
| B. | 原子半径:X<Y | |
| C. | Z的非金属性比Y的强 | |
| D. | X与Y形成的化合物都易溶于水 |
12.已知混合粉末25g,与足量盐酸充分反应后,得到标况下的H2 11.2L,则下列各组金属可能是( )
| A. | Mg和Zn | B. | Zn和Fe、C | C. | Cu和Fe | D. | Zn和Cu |
9.下列各组离子能大量共存,当溶液中c(H+)=10-1mol/L时,有气体产生;而当溶液中c(H+)=10-13mol/L时,又能生成沉淀.该组离子可能是( )
| A. | Na+、Cu2+、NO3-、CO32- | B. | Ba2+、K+、Cl-、HCO3- | ||
| C. | Fe2+、Na+、SO42-、NO3- | D. | Mg2+、NH4+、SO42-、Cl- |
10.下列说法正确的是( )
| A. | 物质燃烧一定是放热反应 | |
| B. | 断开反应物中的化学键要放出能量 | |
| C. | 放热的化学反应不需要加热都能发生 | |
| D. | 化学反应除了生成新的物质外,还伴随着能量的变化 |