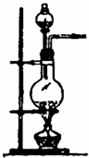
题目内容
欲除去下列物质中混有的少量杂质﹙括号内的物质﹚,写出应加入的试剂及有关反应的方程式.
①Fe2O3(Al2O3)试剂 化学方程式
②NaCl溶液﹙Na2SO4﹚试剂 离子方程式
③FeCl3溶液 ( FeCl2) 试剂 离子方程式 .
①Fe2O3(Al2O3)试剂
②NaCl溶液﹙Na2SO4﹚试剂
③FeCl3溶液 ( FeCl2) 试剂
考点:物质分离、提纯的实验方案设计,离子方程式的书写,常见金属元素的单质及其化合物的综合应用
专题:几种重要的金属及其化合物
分析:(1)Al2O3可与氢氧化钠溶液反应而除去;
(2)可加入适量氯化钡除杂;
(3)可加入氯水除杂.
(2)可加入适量氯化钡除杂;
(3)可加入氯水除杂.
解答:
解:(1)Fe2O3不与氢氧化钠溶液反应,而Al2O3能和氢氧化钠溶液反应化学方程式:Al2O3+2NaOH═2NaAlO2+H2O,故答案为:NaOH;Al2O3+2NaOH═2NaAlO2+H2O;
(2)除去硫酸根又不引入新离子的试剂是氯化钡,反应实质为:Ba2++SO42-=BaSO4↓,故答案为:BaCl2;Ba2++SO42-=BaSO4↓;
(3)氯气与FeCl2反应生成氯化铁,则选择试剂为Cl2,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故答案为:Cl2;2Fe2++Cl2═2Fe3++2Cl-.
(2)除去硫酸根又不引入新离子的试剂是氯化钡,反应实质为:Ba2++SO42-=BaSO4↓,故答案为:BaCl2;Ba2++SO42-=BaSO4↓;
(3)氯气与FeCl2反应生成氯化铁,则选择试剂为Cl2,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故答案为:Cl2;2Fe2++Cl2═2Fe3++2Cl-.
点评:本题考查离子反应方程式的书写,为高频考点,侧重除杂及离子反应的考查,把握物质的性质差异及分离方法为解答的关键,题目难度不大.

练习册系列答案
相关题目
下列除杂方法不正确的是( )
| A、除去乙酸乙酯中混有的少量乙酸:加入饱和碳酸钠溶液,振荡、静置、分液 |
| B、除去乙醇中混有的少量水:加入适量的金属钠,充分反应后蒸馏 |
| C、除去溴苯中混有的少量溴:加入足量的氢氧化钠溶液,振荡、静置、分液 |
| D、除去96%的乙醇中的少量水制无水乙醇:加入生石灰,振荡、静置、蒸馏 |
下列现象或事实可用同一原理解释的是( )
| A、氯化钠和氯化镁溶液分别与硝酸银溶液混合都能产生白色沉淀 |
| B、浓硫酸和稀盐酸长期暴露在空气中浓度降低 |
| C、氯水和活性炭使红墨水褪色 |
| D、漂白粉和水玻璃长期暴露在空气中变质 |
下列物质既能与盐酸又能与氢氧化钠反应的是( )
①Al2O3 ②Al(OH)3 ③NaHCO3 ④Fe ⑤CaCO3 ⑥SiO2.
①Al2O3 ②Al(OH)3 ③NaHCO3 ④Fe ⑤CaCO3 ⑥SiO2.
| A、①②③ | B、①②⑥ |
| C、④⑤⑥ | D、②③⑤ |
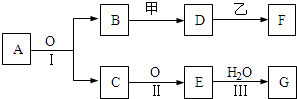
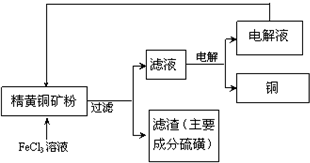 工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.
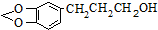 是一种合成药物的中间体,以CH2(COOH)2、CH2Cl2 及
是一种合成药物的中间体,以CH2(COOH)2、CH2Cl2 及 (无机试剂任用)为原料制备该化合物,请将合成该化合物路线流程图补充完整.
(无机试剂任用)为原料制备该化合物,请将合成该化合物路线流程图补充完整.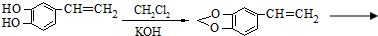
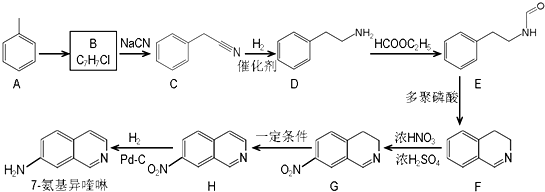
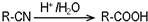 .请回答下列问题:
.请回答下列问题: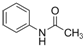 ),请设计合成路线(无机试剂及溶剂任选).
),请设计合成路线(无机试剂及溶剂任选).