题目内容
下列有关物质结构的表述正确的是( )
| A、次氯酸的结构式:H-Cl-O | ||
B、中子数为20的氯原子:
| ||
C、四氯化碳的电子式: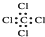 | ||
D、Cl-的结构示意图: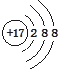 |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,质子数、中子数、核外电子数及其相互联系
专题:
分析:A.次氯酸中存在1个氢氧键和1个氧氯键,不存在氢氯键;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
C.Cl原子最外层达到8电子稳定结构,漏掉了Cl原子的6个电子;
D.氯离子的核电荷数为17,最外层达到8个稳定结构.
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
C.Cl原子最外层达到8电子稳定结构,漏掉了Cl原子的6个电子;
D.氯离子的核电荷数为17,最外层达到8个稳定结构.
解答:
解:A.次氯酸中不存在氢氯键,次氯酸分子中存在1个H-O键和1个Cl-O键,其正确的结构式为:H-O-Cl,故A错误;
B.氯原子的质子数为17,中子数为20的氯原子的质量数为37,该氯原子正确表示方法为:1737Cl,故B错误;
C.四氯化碳中C、Cl原子最外层都达到8电子稳定结构,四氯化碳正确的电子式为: ,故C错误;
,故C错误;
D.氯离子的核电荷数为17,核外电子总数为18,氯离子的结构示意图为: ,故D正确;
,故D正确;
故选D.
B.氯原子的质子数为17,中子数为20的氯原子的质量数为37,该氯原子正确表示方法为:1737Cl,故B错误;
C.四氯化碳中C、Cl原子最外层都达到8电子稳定结构,四氯化碳正确的电子式为:
 ,故C错误;
,故C错误;D.氯离子的核电荷数为17,核外电子总数为18,氯离子的结构示意图为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握结构式、电子式、粒子结构示意图、元素符号的表示方法,C为易错点,注意明确甲烷与四氯化碳电子式的区别.

练习册系列答案
相关题目
室温下,pH相同体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
| A、加水稀释2倍后,两溶液的pH均减小 |
| B、使温度都升高20℃后,两溶液的pH均不变 |
| C、加适量的醋酸钠晶体后,两溶液的pH均增大 |
| D、加足量的锌充分反应后,醋酸产生的氢气比盐酸少 |
实验证明:若用电解熔融KCl制钾,发现钾熔于熔融KCl中难分离,且电解过程中容易发生爆炸事故等.因而工业不用电解熔融KCl制钾,而用金属钠与KCl共熔置换制钾:
Na(l)+KCl(l)?NaCl(l)+K(g)△H>0. 下面是四种物质的熔沸点:
根据平衡移动原理,可推知用Na与KCl反应制取金属钾的适宜温度是( )
Na(l)+KCl(l)?NaCl(l)+K(g)△H>0. 下面是四种物质的熔沸点:
| K | Na | KCl | NaCl | |
| 熔点/℃ | 63.6 | 97.8 | 770 | 801 |
| 沸点/℃ | 774 | 882.9 | 1500 | 1413 |
| A、低于770℃ |
| B、约850℃? |
| C、高于882.9℃ |
| D、1413~1500℃? |
常温常压条件下,下列各组微粒在指定溶液中一定能大量共存的是( )
| A、能和金属铁反应生成H2的溶液中:Fe2+、NO3-、C1-、Na+ |
| B、滴加酚酞显红色的溶液中:Ca2+、K+、SO42-、HCO3- |
| C、无色的酸性溶液中:NH4+、Al3+、NO3-、Cl- |
| D、c(Fe3+)=0.1mol?L-1的溶液中:K+、ClO-、NO3-、SCN- |
一定温度下,将0.1mol HI置于1L某密闭烧瓶中发生反应:2HI(g)?H2(g)+I2(g),下列结论不能说明上述反应达到平衡状态的是( )
| A、烧瓶内气体的颜色不再加深 |
| B、HI的消耗速率与H2的消耗速率之比为2:1 |
| C、I2的生成速率与I2的消耗速率相等 |
| D、烧瓶内气体的质量不变 |
下列说法正确的是( )
| A、若原子X的质子数为a,则X的质量数一定不为a |
| B、若两种元素形成的离子M2-和N+电子层结构相同,则离子半径M2->N+ |
| C、同周期非金属氧化物对应水化物酸性从左到右依次增强 |
| D、由两种元素组成的化合物,若含有离子键,就没有共价键 |
某溶液中含有下列离子中的若干种,K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且各种离子的物质的量浓度相等.现取三份溶液进行如下实验:
①第一份溶液:加入BaCl2溶液,有白色沉淀生成.
②第二份溶液:用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察,没有紫色火焰.
③第三份溶液:加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液中阴离子种类不变.根据上述实验,以下推测正确的是( )
①第一份溶液:加入BaCl2溶液,有白色沉淀生成.
②第二份溶液:用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察,没有紫色火焰.
③第三份溶液:加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液中阴离子种类不变.根据上述实验,以下推测正确的是( )
| A、步骤①中的白色沉淀为2种钡盐 |
| B、溶液中难以确定Cl-的存在与否 |
| C、原溶液中所含的离子有5种 |
| D、步骤③中可以确定Fe2+、NO3-的存在,不能确定其它离子是否存在 |