题目内容
2.一支50mL酸式滴定管中盛盐酸,液面恰好在3.10mL刻度处,把管内液体全部放出,所得液体体积是( )| A. | 3.10 mL | B. | (50-3.10)mL | C. | 大于(50-3.10)mL | D. | 大于3.10mL |
分析 滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,量筒与此相反,据此即可解答.
解答 解:滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,50mL滴定管中实际盛放液体的体积大于50ml,因此,一支50mL酸式滴定管中盛盐酸,液面恰好在3.10mL刻度处,把管内液体全部放出,还有满刻度以下的溶液一并放出,总量超过(50-3.10)ml,盛入量筒内,所得液体体积一定是大于(50-3.10)mL,
故选C.
点评 本题考查了酸式滴定管的结构,注意滴定管的“0”刻度在上端,满刻度在下端,滴定管满刻度以下还有一段空间没有刻度,是解答的关键,题目难度不大.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
12.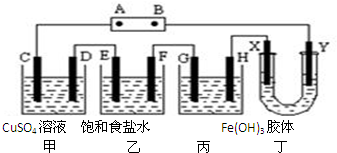 将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )
将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )
 将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )
将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )| A. | 电源B 极的名称是负极,丁中Y极附近颜色变深 | |
| B. | 乙装置中电解一段时间后,加入0.2mol盐酸则可以恢复原来的浓度 | |
| C. | 设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为0.2mol/L | |
| D. | 甲装置中电解反应的总化学方程式是:CuSO4+Fe$\frac{\underline{\;电解\;}}{\;}$Cu+FeSO4 |
13.下列关于钠的叙述错误的是( )
| A. | 实验后剩余少量钠可放回原试剂瓶中 | |
| B. | 用一般的化学还原法不能制取金属钠 | |
| C. | 某物质的焰色反应为黄色,则该物质一定含钠元素 | |
| D. | 钠可以用少量水密封保存 |
10.下列说法正确的是( )
| A. | 将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 | |
| B. | 用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 | |
| C. | 用水可以鉴别乙醇、甲苯和溴苯 | |
| D. | 用酸性高锰酸钾溶液可以鉴别苯、环已烯和环已烷 |
14.下列物质除杂(括号内物质为杂质)所用试剂正确的是( )
| 物 质 | 试 剂 | |
| A | Na2SO4溶液(NaBr) | Cl2 |
| B | FeCl2 溶液(FeCl3) | Cu |
| C | CO2(CO) | 通入O2燃烧 |
| D | CO2(HCl) | 饱和NaHCO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
11.某只含有C、H、O、N的有机物的简易球棍模型如图所示,下列关于该有机物的说法不正确的是( )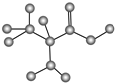

| A. | 该有机物属于氨基酸 | |
| B. | 该有机物的分子式为C3H7NO2 | |
| C. | 该有机物与CH3CH2CH2NO2互为同分异构体 | |
| D. | 一定条件下不能生成高分子化合物 |
12.金属钠与下列物质的溶液反应,既有沉淀生成又有气体放出的是( )
| A. | Mg(NO3)2 | B. | HNO3 | C. | Na2SO4 | D. | NH4Cl |