题目内容
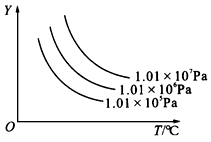
下图所示,是表示外界条件(温度、压强)的变化对下列反应的影响:L(s)+G(g)![]() 2R(g)(正反应为吸热反应),在下图中,Y轴是指( )
2R(g)(正反应为吸热反应),在下图中,Y轴是指( )
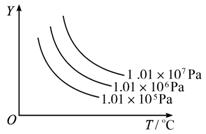
A.平衡混合气中G的百分含量 B.平衡混合气中R的百分含量
C.G的转化率 D.L的转化率
解析:根据题中给出的反应式可知,该反应是一个气体体积增大的吸热反应。
根据图形曲线可知,Y所指的量应该是:
“随温度的升高而减小”以及“随压强的增大而增大”者,应由此来判断符合题意的选项。
升温使题中的平衡反应右移,所以R%增大,G%减小,L和G的转化率都增大,故只有选项A符合要求。
增大压强,使平衡左移,R%减少,G%增大,也是A符合要求,所以Y轴是指平衡混合气体中G的百分含量。
答案:A

|
下图所示,是表示外界条件(温度、压强)的变化对下列反应的影响:L(s)+G(g)
| |
A. |
平衡混合气中G的百分含量 |
B. |
平衡混合气中R的百分含量 |
C. |
G的转化率 |
D. |
L的转化率 |
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
|
编号 |
操作 |
实验现象 |
|
① |
分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 |
试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
|
② |
另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 |
试管A、B中均未明显见到有气泡产生。 |
(1)过氧化氢分解的化学方程式为_____________________________________。
(2)实验①的目的是_________________________________________________。
实验中滴加FeCl3溶液的目的是_______________________________________。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_______________________(用实验中所提供的几种试剂)。
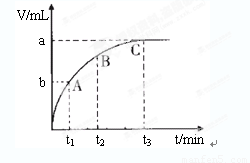
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,则A、B、C三点所表示的瞬时反应速率最慢的是______。

为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
|
编号 |
操作 |
实验现象 |
|
① |
分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 |
试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
|
② |
另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 |
试管A、B中均未明显见到有气泡产生。 |
(1)过氧化氢分解的化学方程式为__________________________________________。
(2)实验①的目的是______________________________________________________。实验中滴加FeCl3溶液的目的是_________________________________________。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是__________________________________(用实验中所提供的几种试剂)。
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,则A、B、C三点所表示的瞬时反应速率最慢的是______________________。
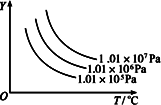
 2R(g)(正反应为吸热反应),在下图中,y轴是指
2R(g)(正反应为吸热反应),在下图中,y轴是指