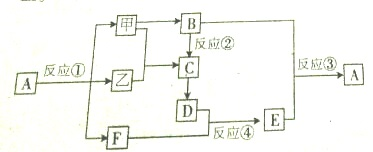
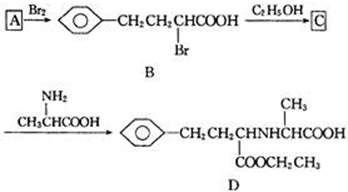
题目内容
现有70g质量分数为70%的硫酸和50g含杂质20%的烧碱(杂质不参加反应),足量的铝屑.用上述原料生产Al(OH)3的量最多时消耗铝的质量为( )
| A、26g | B、36g |
| C、104g | D、130g |
考点:化学方程式的有关计算
专题:计算题
分析:铝与硫酸反应生成硫酸铝、铝与氢氧化钠反应生成偏铝酸钠,然后根据铝离子与偏铝酸根离子发生双水解得到的氢氧化铝的量最大,由此分析解答.
解答:
解:根据金属铝和酸以及和碱发生反应的化学方程式可以得出:Al~3H+~Al3+~
H2SO4~Al(OH)3,
Al~OH-~NaOH~[Al(OH)4]-,由可知Al3++3[Al(OH)4]-=4Al(OH)3↓,Al3+~3[Al(OH)4]-~
H2SO4~3NaOH~4Al(OH)3↓,所以
H2SO4 ~3NaOH~4Al(OH)3↓,
3 4
经比较硫酸过量,所以根据氢氧化钠来求生成氢氧化铝的质量:
=
,氢氧化铝的质量为:
×78=26g,故选A.
| 3 |
| 2 |
Al~OH-~NaOH~[Al(OH)4]-,由可知Al3++3[Al(OH)4]-=4Al(OH)3↓,Al3+~3[Al(OH)4]-~
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 70g×70% |
| 98g/mol |
| 50g×20% |
| 40g/mol |
经比较硫酸过量,所以根据氢氧化钠来求生成氢氧化铝的质量:
| 3 |
| 0.25 |
| 4 |
| n(氢氧化铝) |
| 1 |
| 3 |
点评:本题考查学生由金属铝制得氢氧化铝的实验方案知识,是一道工业生产和化学结合的题目,难度较大.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
有关下列说法错误的是( )
| A、工厂里采用静电除尘,是利用了胶体电泳的性质 |
| B、根据物质在水中或熔融状态下是否导电,可将其分为电解质和非电解质 |
| C、分析和实验也是研究物质性质的方法 |
| D、电解质在水溶液中的反应实质是离子间的反应 |
下列关于物质分类的说法不正确的是( )
| A、冰和干冰既是纯净物又是化合物 |
| B、CuSO4?5H2O属于纯净物 |
| C、纯碱和熟石灰都是碱 |
| D、豆浆和雾都是胶体 |
稀释某弱酸HA溶液时,浓度增大的是( )
| A、HA |
| B、H+ |
| C、A- |
| D、OH- |
海水是一个巨大的化学资源库,下列有关海水综合利用的说法错误的是( )
| A、海水中含有溴元素,需经过化学变化才可以得到溴单质 | ||||||||
| B、无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能 | ||||||||
| C、从海水中可以得到NaCl,电解熔融NaCl可制备金属钠 | ||||||||
D、从海水中提取镁可以采用下列方法:海水海水
|
恒温、恒压下,1mol A和n mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成a mol C.则下列说法正确的是( )
| A、物质A的转化率为a | ||
B、起始时刻和达到平衡时容器中的压强比为(1+n):(1+n-
| ||
| C、反应达平衡后,再向容器中充入amolHe,物质B的转化率减小 | ||
| D、当v正(A)=2v逆(C)时,可判断反应达到平衡 |