题目内容
11.下列有关说法正确的是( )| A. | 蛋白质、淀粉、纤维素、葡萄糖等都能在人体内水解并提供能量 | |
| B. | 将甲烷和乙烯的混合气体通过盛有溴水的洗气瓶,即可提纯甲烷 | |
| C. | C2H6与氯气发生取代反应,C2H4与HCl发生加成反应,均可得到C2H5Cl | |
| D. | 用溴水一种试剂就可将苯、CCl4、乙酸、乙醇区别 |
分析 A.纤维素不能在人体内水解;
B.乙烯可与溴水发生加成反应;
C.C2H6与氯气的取代反应可生成多种氯代烃;
D.乙酸、乙醇与溴水都不反应,且易溶于水.
解答 解:A.人体内不含纤维素酶,纤维素不能在人体内水解,故A错误;
B.乙烯可与溴水发生加成反应,可用于除杂,故B正确;
C.C2H6与氯气的取代反应可生成多种氯代烃,得到混合物,故C错误;
D.乙酸、乙醇与溴水都不反应,且易溶于水,不能够鉴别,故D错误.
故选B.
点评 本题多角度考查有机物的结构和性质,为高考常见题型,侧重学生的分析能力的考查,有利于双基的夯实,注意把握有机物的组成、结构和官能团的性质,难度不大.

练习册系列答案
相关题目
2. 氮元素的化合物种类繁多,性质也各不相同.
氮元素的化合物种类繁多,性质也各不相同.
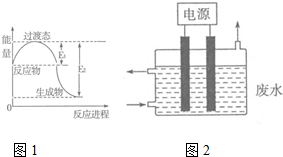
(1)图1为一定温度下1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图.已知E1=147.5kJ•mol-1,E2=376.2kJ•mol-1(E1、E2为反应的活化能).若在反应体系中加入催化剂,反应速率增大,则E1减小(填“增大”、“减小”或“不变”).该反应的热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-228.7KJ/mol.
(2)硝基苯甲酸乙酯在OH-存在的条件下发生水解反应:
O2NC6H4COOC2H5+OH-?O2NC6H4COOO-+C2H5OH
两种反应物的初始浓度均为0.050mol•L-1,某温度下测得O2NC6H4COOC2H5的转化率α随时间变化的数据如下表所示:
回答下列问题:①该反应在330s~530s的平均反应速率为$\frac{0.05×(73%-59%)}{200}$(只列算式,不做运算)
②为提高O2NC6H4COOC2H5的转化率,可以采取的措施有增加OH-的浓度、移去产物. (写1条即可)
(3)2015年8月12日天津港爆炸中有一定量的氰化物泄露,可用如图2所示装置除去含CN-、Cl-废水中的CN-,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,该反应的离子方程式为2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-,,其中两个电极的材料分别为石墨和铁,则石墨作阳极,其电极反应式为Cl-+2OH--2e-═ClO-+H2O.
 氮元素的化合物种类繁多,性质也各不相同.
氮元素的化合物种类繁多,性质也各不相同.(1)图1为一定温度下1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图.已知E1=147.5kJ•mol-1,E2=376.2kJ•mol-1(E1、E2为反应的活化能).若在反应体系中加入催化剂,反应速率增大,则E1减小(填“增大”、“减小”或“不变”).该反应的热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-228.7KJ/mol.
(2)硝基苯甲酸乙酯在OH-存在的条件下发生水解反应:
O2NC6H4COOC2H5+OH-?O2NC6H4COOO-+C2H5OH
两种反应物的初始浓度均为0.050mol•L-1,某温度下测得O2NC6H4COOC2H5的转化率α随时间变化的数据如下表所示:
| t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
| α/% | 0 | 33 | 42 | 49 | 59 | 73 | 74 | 75 | 75 |
②为提高O2NC6H4COOC2H5的转化率,可以采取的措施有增加OH-的浓度、移去产物. (写1条即可)
(3)2015年8月12日天津港爆炸中有一定量的氰化物泄露,可用如图2所示装置除去含CN-、Cl-废水中的CN-,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,该反应的离子方程式为2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-,,其中两个电极的材料分别为石墨和铁,则石墨作阳极,其电极反应式为Cl-+2OH--2e-═ClO-+H2O.
6.某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成,取适量该溶液进行如下实验:
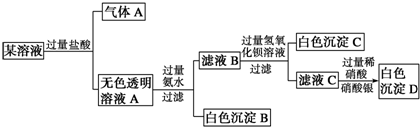
下列说法正确的是( )

下列说法正确的是( )
| A. | 原溶液中一定只存在AlO2-、CO32-、SO42-、Cl-四种离子 | |
| B. | 原溶液中是否存在Na+无法判断 | |
| C. | 原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+ | |
| D. | 生成沉淀B的离子方程式为:Al3++3OH-═Al(OH)3↓ |
16.下列说法不正确的是( )
| A. | 用铜作电极电解NaCl溶液,可以实现反应:Cu+2H2O$\frac{\underline{\;电解\;}}{\;}$Cu(OH)2↓+H2↑ | |
| B. | 用铜、铝作电极与电解质溶液构成原电池时,铜一定是正极 | |
| C. | N2O4和NO2混合气体69g,完全与水反应转移电子数约为6.02×1023 | |
| D. | HCl和HS-均是含有一个极性键的18电子粒子 |
20.检验溴乙烷中是否有溴元素,合理的实验方法是( )
| A. | 加入氯水后振荡,看水层里是否有棕红色的溴出现 | |
| B. | 加入硝酸银溶液,再加稀硝酸,观察有无浅黄色沉淀生成 | |
| C. | 加入NaOH水溶液共热,冷却后加硝酸银溶液,观察有无浅黄色沉淀生成 | |
| D. | 加入NaOH水溶液共热,冷却后用过量稀硝酸中和过量碱后,再加硝酸银溶液,观察有无浅黄色沉淀生成 |
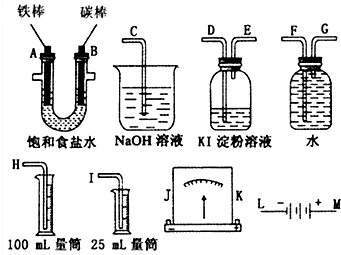 某课外小组做电解食盐水的探究实验,现有如图所示所列实验装置,请从其中选择适当的装置并加以组装,要求检验氯气的氧化性,并测定产生氢气的体积.
某课外小组做电解食盐水的探究实验,现有如图所示所列实验装置,请从其中选择适当的装置并加以组装,要求检验氯气的氧化性,并测定产生氢气的体积.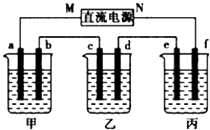 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g500%的NaOH溶液、足量的CuSO4溶液和l00g10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g500%的NaOH溶液、足量的CuSO4溶液和l00g10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题: