题目内容
17.向含有1molFeSO4和1molAlBr3的混合溶液中加入下列物质,离子方程式书写正确的是( )| A. | 通入1molCl2:2Fe2++2Br-+2Cl2→4Cl-+Br2+2Fe3+ | |
| B. | 通入足量Cl2:2Fe2++4Br-+3Cl2→2Fe3++2Br2+6Cl- | |
| C. | 加入含2molBa(OH)2的溶液:Al3++SO42-+Ba2++4OH-→BaSO4↓+AlO2-+2H2O | |
| D. | 加入足量Ba(OH)2的溶液:Fe2++Al3++SO42-+Ba2++6OH-→Fe(OH)2↓+AlO2-+BaSO4↓+2H2O |
分析 A.由还原性及电子守恒可知,只有亚铁离子被氧化;
B.足量氯气,亚铁离子、溴离子均被氧化;
C.碱不足,生成硫酸钡和氢氧化亚铁;
D.加入足量Ba(OH)2的溶液,生成硫酸钡、氢氧化亚铁、偏铝酸钡、水.
解答 解:A.由还原性及电子守恒可知,只有亚铁离子被氧化,则通入1molCl2的离子反应为2Fe2++2Br-+2Cl2→4Cl-+Br2+2Fe3+,故A正确;
B.足量氯气,亚铁离子、溴离子均被氧化,则通入足量Cl2离子反应为2Fe2++6Br-+4Cl2→2Fe3++3Br2+8Cl-,故B错误;
C.碱不足,生成硫酸钡和氢氧化亚铁、氢氧化铝,则加入含2molBa(OH)2的溶液的离子反应为Fe2++SO42-+Ba2++2OH-→BaSO4↓+Fe(OH)2↓,故C错误;
D.加入足量Ba(OH)2的溶液,生成硫酸钡、氢氧化亚铁、偏铝酸钡、水,则加入足量Ba(OH)2的溶液的离子反应为Fe2++Al3++SO42-+Ba2++6OH-→Fe(OH)2↓+AlO2-+BaSO4↓+2H2O,故D正确;
故选AD.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
7.短周期元素X、Y、Z、W的原子序数依次增大.X原子核内没有中子;Z与W在周期表中同主族,且Y、Z和W三种元素的原子最外层电子数之和为17;X、Y形成的化合物M的水溶液呈碱性.则下列说法不正确的是( )
| A. | 原子半径:W>Y>Z>X | |
| B. | 标准状况下的2.24 LM溶于水,所得溶液pH=13 | |
| C. | YZ2能使湿润的淀粉KI试纸变蓝 | |
| D. | 一定条件下,Cu可与W的最高价氧化物对应水化物发生反应 |
8.下列每组物质发生变化所克服的粒子间的作用力属于同种类型的是( )
| A. | 氯化铵受热气化和苯的汽化 | B. | 碘和干冰受热升华 | ||
| C. | 二氧化硅和生石灰的熔化 | D. | 氯化钠和铁的熔化 |
5.下列关于14C的化学用语表示正确的是( )
| A. | 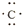 | B. | 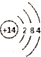 | C. | 1s22s2p4 | D. | 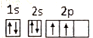 |
12.常温下,将3.9gNa2O2粉末投入水中,充分反应.关于此过程说法正确的是(NA表示阿伏伽德罗常数)( )
| A. | 生成气体体积为560mL | B. | 反应中电子转移数目为0.1NA | ||
| C. | Na2O2粉末中含离子数目为0.15NA | D. | 所得溶液pH为13 |
2.化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( )
| A. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 硅胶可用作食品干燥剂 | |
| C. | “天宫一号”使用的碳纤维,是一种新型有机高分子材料 | |
| D. | 工业上燃烧煤时,加入少量石灰石是为了减少CO2的排放 |
13.下列物质能使品红溶液褪色的是( )
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫.
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫.
| A. | ①③④ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
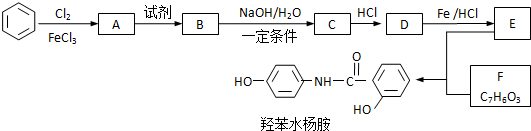
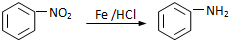
 .
.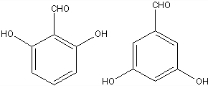 、
、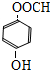 .
.