题目内容
20.下列操作中能使电离平衡H2O?H++OH-,向右移动且溶液呈酸性的是( )| A. | 将水加热到100℃,使pH=6 | B. | 向水中加入Al2(SO4)3固体 | ||
| C. | 向水中加入Na2CO3溶液 | D. | 向水中加入NaHSO4溶液 |
分析 能使电离平衡H2O?H++OH-向右移动,说明加入的物质能和氢离子或氢氧根离子反应而促进水的电离;溶液呈酸性,说明加入的物质和氢氧根离子反应,导致溶液中氢氧根离子浓度小于氢离子浓度而使溶液呈酸性,据此进行分析.
解答 解:A、升高温度,水的电离程度增大,但是溶液中氢离子浓度等于氢氧根离子浓度,溶液显示中性,故A错误;
B、向水中加入硫酸铝,铝离子水解而促进水电离,且溶液呈酸性,故B正确;
C、向水中加入碳酸钠溶液,碳酸根离子水解促进水的电离,碳酸根离子和氢离子结合生成碳酸氢根离子而使溶液中氢氧根离子浓度大于氢离子浓度,所以溶液呈碱性,故C错误;
D、硫酸氢钠的电离:NaHSO4═Na++H++SO42-,溶液中氢离子浓度增大,水的电离平衡向着逆向移动,故D错误;
故选B.
点评 本题考查影响水电离的因素,注意不能根据pH确定溶液是酸碱性,要根据氢离子浓度和氢氧根离子浓度的相对大小确定溶液的酸碱性,题目难度不大.

练习册系列答案
相关题目
20.如图是石蜡油(液态烷烃混合物)在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验.下列有关说法错误的是( )
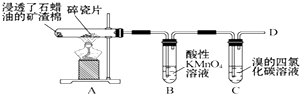

| A. | A装置中碎瓷片的作用是做催化剂 | B. | B、C试管中的溶液均要褪色 | ||
| C. | B、C试管中均发生的是加成反应 | D. | 在D处点燃前,一定要先验纯 |
1.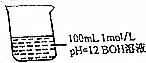 常温下对图中溶液分别进行下列操作,相关分析正确的是( )
常温下对图中溶液分别进行下列操作,相关分析正确的是( )
 常温下对图中溶液分别进行下列操作,相关分析正确的是( )
常温下对图中溶液分别进行下列操作,相关分析正确的是( )| A. | 稀释10倍,溶液中n(H+)•n(OH-)不变 | |
| B. | 加人100mL pH=2的盐酸,溶液中存在c(Cl-)=c(B+) | |
| C. | 加入少量BCl固体,固体溶解后溶液pH不变(忽略溶液体积变化) | |
| D. | 若升高温度,$\frac{c({B}^{+})+c({H}^{+})}{c(0{H}^{-})}$保持不变 |
8.下列关于化学键的说法,正确的是( )
| A. | 由非金属元素组成的化合物不一定是共价化合物 | |
| B. | 离子化合物可能含共价键,共价化合物可能含离子键 | |
| C. | 任何单质中一定含共价键 | |
| D. | 离子键的本质就是阴阳离子间的静电引力 |
5.下列关于乙醇的说法正确的是( )
| A. | 能用作汽车燃料 | B. | 能腐蚀铁制容器 | ||
| C. | 能与NaOH溶液反应 | D. | 能被Cu催化氧化成C02 |
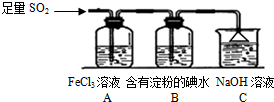 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示: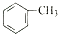 ;b.CH≡CCH3; c、
;b.CH≡CCH3; c、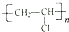
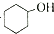 和
和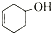 ,可选用b(填字母)
,可选用b(填字母)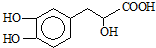
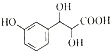 )与足量溴水反应所得产物的结构简式为
)与足量溴水反应所得产物的结构简式为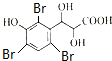 .
.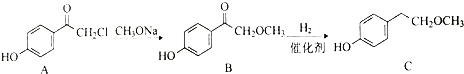
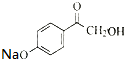 .
. .
.