题目内容
下列各组离子中,能在强酸性溶液中大量共存的是( )
| A、Na+ K+ SO42- OH- |
| B、Na+ K+ Cl- HCO3- |
| C、Na+Cu2+ CO32- Br- |
| D、Na+ Mg2+ NO3- Cl- |
考点:离子共存问题
专题:离子反应专题
分析:强酸性溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,不能发生氧化还原反应,则离子大量共存,以此来解答.
解答:
解:A.H+、OH-结合生成水,不能大量共存,故A不选;
B.H+、HCO3-结合生成水和气体,不能共存,故B不选;
C.H+、CO32-结合生成水和气体,且CO32-、Cu2+结合生成沉淀,不能共存,故C不选;
D.该组离子在酸性溶液中不反应,可大量共存,故D选;
故选D.
B.H+、HCO3-结合生成水和气体,不能共存,故B不选;
C.H+、CO32-结合生成水和气体,且CO32-、Cu2+结合生成沉淀,不能共存,故C不选;
D.该组离子在酸性溶液中不反应,可大量共存,故D选;
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
不属于烃类的有机物是( )
| A、CH3COOH |
| B、CH2=CH2 |
| C、CH3CH2OH |
| D、CH3COOCH2CH3 |
下列物质转化在给定条件下能实现的是( )
①FeS2
SO3
H2SO4→CO2
②Al2O3
NaAlO2(aq)→Al(OH)3
③NaCl(aq)
Na→NaOH(aq)
④Fe
FeSO4(aq)→Fe(OH)2
Fe2O3
⑤海水
母液
NaBrO3
粗溴
Br2.
①FeS2
| 煅烧 |
| H2O |
②Al2O3
| NaOH(aq) |
③NaCl(aq)
| 电解 |
④Fe
| 稀H2SO4 |
| 空气中灼烧 |
⑤海水
| 蒸发 |
| 提取NaCl |
| Na2CO3(aq) |
| Cl2 |
| 热空气 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
反应A+3B2C+2D在四种不同时刻的反应速率分别为:
①v (A)=0.15mol/(L?min)
②v (B)=0.6mol/(L?min)
③v(C)=0.45mol/(L?min)
④v(D)=0.40mol/(L?min),则这四个时段的速率由快至慢的顺序为( )
①v (A)=0.15mol/(L?min)
②v (B)=0.6mol/(L?min)
③v(C)=0.45mol/(L?min)
④v(D)=0.40mol/(L?min),则这四个时段的速率由快至慢的顺序为( )
| A、①>②>③>④ |
| B、③>④=②>① |
| C、②>①>③>④ |
| D、①>②=③>④ |
一氯化碘(ICl)、三氯化碘(ICl3)是卤素互化物,它们的性质与卤素单质相似,如:2ICl+2Zn═ZnI2+ZnCl2.以下判断正确的是( )
| A、ICl3与水反应的产物为HI和HClO |
| B、ICl3与KI反应时,氯元素被还原 |
| C、ICl与冷NaOH溶液反应的离子方程式为:ICl+2OH-=IO-+Cl-+H2O |
| D、ICl与水的反应属于氧化还原反应 |
叠氮酸(HN3)与醋酸的酸性相似,0.2mol HN3与0.2molNaOH反应后将溶液稀释至500mL,测得溶液pH=α,下列说法一定错误的是( )
| A、HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-) |
| B、题示500mL溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) |
| C、题示500mL溶液中由水电离产生的c(OH-)=1×10-αmol?L-1 |
| D、根据题给出的数据可以计算该温度喜爱叠氮酸的电离平衡常数Kα |
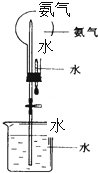 哈伯因为氨气的合成曾获1918年诺贝尔奖.
哈伯因为氨气的合成曾获1918年诺贝尔奖.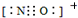
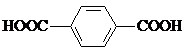 )、4,4′-联吡啶
)、4,4′-联吡啶 (可简化为
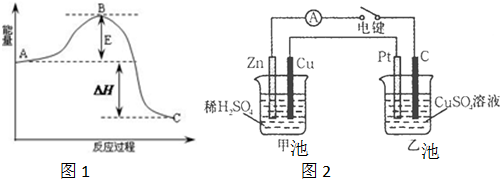
(可简化为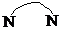 )等与Ni2+能形成多核配合物.配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如图2:
)等与Ni2+能形成多核配合物.配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如图2: