题目内容
18.对下列装置图或图象描述正确的是( )
| A. | 作为测量中和反应反应热的装置图,从玻璃仪器的角度看,图1还缺少环形玻璃搅拌棒 | |
| B. | 检验图2装置的气密性时,向漏斗中加水若出现图中所示的现象,可以证明该气密性良好 | |
| C. | 已知图3是利用原电池检验空气中Cl2含量的装置,其中Pt电极作负极 | |
| D. | 根据图4的溶解度变化可知,在较低温度下容易分离MgSO4•7H2O和CaSO4•2H2O |
分析 A.大小烧杯口应相平,可防止热量散失;
B.检验图2装置的气密性时,利用液柱法检验气密性即可;
C.由2Ag+Cl2=2AgCl及装置可知,Ag失去电子作负极;
D.由图可知,温度高于40℃时MgSO4•7H2O和CaSO4•2H2O溶解度差异较大.
解答 解:A.大小烧杯口应相平,可防止热量散失,且图1还缺少环形玻璃搅拌棒,故A错误;
B.检验图2装置的气密性时,关闭止水夹,向漏斗中加水若出现图中所示的现象,且一段时间液柱高度不变,则可以证明该气密性良好,故B正确;
C.由2Ag+Cl2=2AgCl及装置可知,Ag失去电子作负极,而Pt电极作正极,故C错误;
D.由图可知,温度高于40℃时MgSO4•7H2O和CaSO4•2H2O溶解度差异较大,则在较高温度下容易分离MgSO4•7H2O和CaSO4•2H2O,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,侧重于学生的分析能力与实验能力的考查,注意把握中和热测定实验、气密性检验、原电池及溶解度等为解答的关键,题目难度中等.

练习册系列答案
相关题目
3.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 16 g O2中含有的氧分子数为NA | |
| B. | 1 mol Mg变为Mg2+时失去的电子数目为2NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 1 mol•L-1 CaCl2溶液中含有的氯离子数为NA |
10.以下名称、化学用语均正确的是( )
| A. | 笨的实验式:CH | B. | 二氯乙稀的结构简式:CH2=C(Cl)2 | ||
| C. | 甲酸的结构式: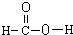 | D. | 醛基的电子式: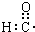 |
7.在体积固定,容积为2L的密闭容器中进行如下化学反应:
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应一定达到化学平衡状态的依据是BC.
A.容器中压强不再改变 B.混合气体中c(CO)不再改变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为
2mol/L,c(H2)为1.5mol/L,c(CO)为1mol/L,c(H2O)为3mol/L,则下一时刻,反应向逆向(填“正向”或“逆向”)进行.
(5)保持容器体积不变,下列措施中一定能使H2的转化率增大的有CD.
A.充入氦气
B.使用催化剂
C.平衡后再向容器内通入一定量CO2
D.升高温度
(6)在830℃时,发生上述反应,若开始时加入0.3mol CO2和0.2mol H2,经过3分钟刚好达到平衡,以CO的浓度变化表示的化学反应速率为v(CO)=0.02mol•L-1•min-1.
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应一定达到化学平衡状态的依据是BC.
A.容器中压强不再改变 B.混合气体中c(CO)不再改变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为
2mol/L,c(H2)为1.5mol/L,c(CO)为1mol/L,c(H2O)为3mol/L,则下一时刻,反应向逆向(填“正向”或“逆向”)进行.
(5)保持容器体积不变,下列措施中一定能使H2的转化率增大的有CD.
A.充入氦气
B.使用催化剂
C.平衡后再向容器内通入一定量CO2
D.升高温度
(6)在830℃时,发生上述反应,若开始时加入0.3mol CO2和0.2mol H2,经过3分钟刚好达到平衡,以CO的浓度变化表示的化学反应速率为v(CO)=0.02mol•L-1•min-1.
18.NaCl在生产中有重要作用.
(1)某小组用NaCl进行以下实验:
①Ⅰ中白色沉淀的化学式是AgCl.
②Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-,沉淀能发生转化的主要原因是Ag2S比AgCl溶解度更小.
③经检测步骤Ⅲ中乳白色沉淀是AgCl和S的混合物.请写出黑色沉淀变为乳白色的化学方程式2Ag2S+O2+4NaCl+2H2O=4AgCl+2S+4NaOH,从化学平衡移动的角度解释在沉淀变色过程中NaCl的作用Ag2S被O2氧化生成S时释放出Ag+,NaCl中的Cl-与Ag+结合成AgCl沉淀,c(Ag+)减小,③中平衡向正反应方向移动,最终出现乳白色沉淀.
(2)电解法是治理铵盐为主要水体污染物的一种方法,原理是:在污水中加入一定量NaCl进行电解,产生的Cl2与水反应生成HClO,HClO 将NH4+氧化为N2,使水体脱氮.请写出酸性条件下HClO 与NH4+反应的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.研究发现:污水呈弱酸性比强酸性更有利于使NH4+氧化为N2而脱氮,原因是酸性较强时,Cl2+H2O?H++Cl-+HClO 的化学平衡向逆反应方向移动,生成的HClO减少,不利脱氮.
(1)某小组用NaCl进行以下实验:
| 步 骤 | 现 象 |
| Ⅰ.将NaCl溶液与AgNO3溶液混合 | 产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
| Ⅲ.将Ⅱ中经过滤洗得到的黑色沉淀分成两份,在一份沉淀中加蒸馏水,另一份沉淀中加入NaCl溶液,同时浸泡较长时间. | 加蒸馏水的沉淀仍为黑色,加入NaCl溶液的沉淀变为乳白色 |
②Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-,沉淀能发生转化的主要原因是Ag2S比AgCl溶解度更小.
③经检测步骤Ⅲ中乳白色沉淀是AgCl和S的混合物.请写出黑色沉淀变为乳白色的化学方程式2Ag2S+O2+4NaCl+2H2O=4AgCl+2S+4NaOH,从化学平衡移动的角度解释在沉淀变色过程中NaCl的作用Ag2S被O2氧化生成S时释放出Ag+,NaCl中的Cl-与Ag+结合成AgCl沉淀,c(Ag+)减小,③中平衡向正反应方向移动,最终出现乳白色沉淀.
(2)电解法是治理铵盐为主要水体污染物的一种方法,原理是:在污水中加入一定量NaCl进行电解,产生的Cl2与水反应生成HClO,HClO 将NH4+氧化为N2,使水体脱氮.请写出酸性条件下HClO 与NH4+反应的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.研究发现:污水呈弱酸性比强酸性更有利于使NH4+氧化为N2而脱氮,原因是酸性较强时,Cl2+H2O?H++Cl-+HClO 的化学平衡向逆反应方向移动,生成的HClO减少,不利脱氮.
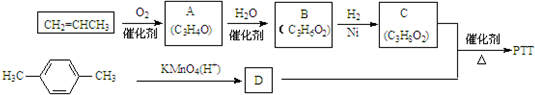
 .①分子式为C4H6O ②含有1个-CH3
.①分子式为C4H6O ②含有1个-CH3 ,反应类型为缩聚反应.
,反应类型为缩聚反应.