题目内容
已知反应:①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O,
②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O,
③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4。下列结论正确的是
A.①②③均是氧化还原反应
B.氧化性强弱顺序是:K2Cr2O7>Fe2(SO4)3>I2
C.反应②中氧化剂与还原剂的物质的量之比为6∶1
D.反应③中0.1mol还原剂共失去电子数为1.2×1022
B
【解析】
试题分析:A、①中元素的化合价均为发生变化,不是氧化还原反应,错误;B、根据氧化还原反应规律,②中的氧化剂是K2Cr2O7,氧化产物是Fe2(SO4)3,所以氧化性K2Cr2O7>Fe2(SO4)3,同理可得③中氧化性的顺序是Fe2(SO4)3>I2,二者结合可得氧化性强弱顺序是:K2Cr2O7>Fe2(SO4)3>I2,正确;C、反应②中氧化剂与还原剂的物质的量之比为1:6,错误;D、反应③中KI是还原剂,0.1mol还原剂共失去电子数为6.02×1022,错误,答案选B。
考点:考查氧化还原反应的判断与计算、规律的应用

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
 中含有的碳碳双键数目为0.3NA
中含有的碳碳双键数目为0.3NA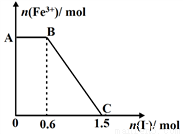
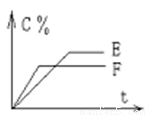
 pC(气) + qD(气)的 C %与时间 t有如图关系
pC(气) + qD(气)的 C %与时间 t有如图关系