题目内容
把SO2通入下列各组物质的混合溶液中,肯定有白色沉淀生成的是( )
| A、Ba(NO3)2、HCl |
| B、BaCl2、NaCl |
| C、NH3?H2O、CaCl2 |
| D、MgCl2、H2SO4 |
考点:二氧化硫的化学性质
专题:
分析:酸性条件下,硝酸盐具有强氧化性,与二氧化硫发生氧化还原反应生成硫酸根离子,可生成硫酸钡沉淀,碱性条件下,可生成亚硫酸盐沉淀,如二氧化硫过量,生成亚硫酸氢盐,以此解答该题.
解答:
解:A.SO2通入Ba(NO3)2、HCl溶液中,发生氧化还原反应生成硫酸钡沉淀,故A选;
B.亚硫酸酸性比盐酸弱,物质之间均不发生反应,不生成沉淀,故B不选;
C.如二氧化硫过量,则生成亚硫酸氢钙,故C不选;
D.亚硫酸酸性比硫酸弱,物质之间均不发生反应,不生成沉淀,故D不选.
故选D.
B.亚硫酸酸性比盐酸弱,物质之间均不发生反应,不生成沉淀,故B不选;
C.如二氧化硫过量,则生成亚硫酸氢钙,故C不选;
D.亚硫酸酸性比硫酸弱,物质之间均不发生反应,不生成沉淀,故D不选.
故选D.
点评:本题考查物质的性质,综合考查元素化合物性质,为高频考点,把握二氧化硫的性质及酸性条件下硝酸盐的强氧化性为解答的关键,注意结合氧化还原反应及酸性强弱分析,题目难度不大.

练习册系列答案
相关题目
核能的和平利用对于完成“节能减排“的目标有着非常重要的意义.尤其是核聚变,因其释放能量大,无污染,成为当前研究的一个热门课题.其反应原理为:
H+
H→
He+
n.下列说法中正确的是( )
2 1 |
3 1 |
4 2 |
1 0 |
| A、D和T是质量数不同,质子数相同的氢的两种元素 | ||||||
B、通常所说的氢元素是指
| ||||||
C、
| ||||||
| D、这个反应既是核反应,也是化学反应 |
在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol/L,加入等体积0.3mol/L的BaCl2溶液恰好使SO42-完全沉淀,则混合溶液中Na+的浓度为( )
| A、0.3 mol/L |
| B、0.45 mol/L |
| C、0.6 mol/L |
| D、0.15 mol/L |
下列热化学方程式中,正确的是( )
| A、甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 |
| B、由N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ?mol-1热化学方程式可知,当反应中转移6NA电子时,反应放出的热小于92.4 kJ |
| C、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 |
| D、在101 kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=-571.6 kJ?mol-1 |
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-═ZnO+H2O:Ag2O+H2O+2e-═2Ag+2OH-.总反应式为:Ag2O+Zn═2Ag+ZnO,下列说法正确的是( )
| A、Zn为正极,Ag2O为负极 |
| B、电解质溶液中,OH-移向Ag2O极 |
| C、原电池工作时,正极区溶液pH值增大 |
| D、原电池工作时,负极区溶液pH值增大 |
 ⑤CCl4
⑤CCl4 +Zn→CH2=CH2+ZnBr2.写出以1,3-丁二烯为原料合成高分子化合物
+Zn→CH2=CH2+ZnBr2.写出以1,3-丁二烯为原料合成高分子化合物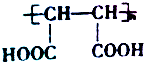 的流程图.
的流程图.