题目内容
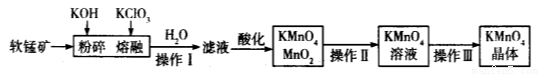
(9分)工业上用软锰矿(主要成分为MnO2)制备高锰酸钾的工艺流程如图所示:
(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强。下列酸能用于酸化高锰酸钾溶液的是____________(填序号)。
A.盐酸 B.稀硫酸 C.硝酸 D.氢硫酸
(2)操作Ⅰ、Ⅱ、Ⅲ的名称分别是______________、_______________、_______________。
(3)软锰矿与过量固体KOH和KClO3在熔融状态下反应时的氧化剂是__________(填化学式)。反应后加水溶解得到的滤液中主要含有KCl和K2MnO4,则滤液酸化时发生反应的离子方程式为______________。
(4)已知KMnO4能与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2。取上述制得的KMnO4产品0.33 g,恰好与0.67 g Na2C2O4完全反应,则KMnO4的纯度为___________________%。
(1)B;(2)过滤;过滤;蒸发;(3)KClO3;3MnO42- + 4H+=2MnO4- + MnO2 + 2H2O;
(4)96或95.76或95.8。
【解析】
试题分析:(1) KMnO4有强氧化性,而盐酸、氢硫酸都有还原性容易被氧化,不能酸化KMnO4;硝酸也有氧化性,也不能酸化KMnO4,因此酸化KMnO4溶液,只能用稀硫酸,故选项是B。(2)操作Ⅰ是分离难溶性固体与可溶性液体混合物的方法,名称为过滤;操作Ⅱ是分离难溶性固体MnO2与可溶性液体KMnO4混合物的方法,名称为过滤;操作Ⅲ是从溶液中分离溶质的方法,名称是蒸发;(3)软锰矿与过量固体KOH和KClO3在熔融状态下反应,KClO3把MnO2氧化为KMnO4,故氧化剂是KClO3。反应后加水溶解得到的滤液中主要含有KCl和K2MnO4,则根据原子守恒、电子守恒、电荷守恒,可得反应的离子方程式为3MnO42-+4H+=2MnO4-+MnO2+2H2O;(4)在氧化还原反应中电子转移数目相等。n(Na2C2O4)= 0.67 g÷134g/mol=0.005mol;n(e-)=0.005mol×2=0.01mol;则n(KMnO4)= 0.01mol÷5=0.002mol,则m(KMnO4)= 0.002mol×158g/mol=0.316g,所以已知KMnO4能与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2。取上述制得的KMnO4产品0.33 g,恰好与Na2C2O4完全反应,则KMnO4的纯度为(0.316g÷0.33 g)×100%=95.76%。
考点:考查分类混合物的方法、物质的氧化性的判断、离子方程式的书写、物质纯度的计算的知识。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案

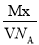 表示的是( )
表示的是( )
