题目内容
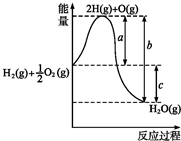 (1)已知:H2(g)+O2(g)═H2O(g),反应过程中能量变化如图所示,则:
(1)已知:H2(g)+O2(g)═H2O(g),反应过程中能量变化如图所示,则:①a、b、c分别代表什么意义?a
②该反应是
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是
(3)已知:H2(g)+O2(g)═H2O(l)△H=-285.8kJ?mol-1H2(g)═H2(l)△H=-0.92kJ?mol-1
O2(g)═O2(l)△H=-6.84kJ?mol-1H2O(l)═H2O(g)△H=+44.0kJ?mol-1请写出液氢和液氧生成气态水的热化学方程式:
考点:反应热和焓变,热化学方程式
专题:化学反应中的能量变化
分析:(1)①依据化学反应的反应热可以根据反应的实质分析,断裂化学键吸收能量,生成化学键放出能量,二者的差值是反应的反应热;
②依据反应物和生成物的能量高低和反应的能量守恒分析判断;
(2)根据氢气燃烧的原理、氢气作为能源的优点分析;
(3)据盖斯定律解答.
②依据反应物和生成物的能量高低和反应的能量守恒分析判断;
(2)根据氢气燃烧的原理、氢气作为能源的优点分析;
(3)据盖斯定律解答.
解答:
解:(1)①图象中可以分析判断,a代表旧键断裂吸收的能量;c为反应生成化学键放出的热量减去反应断裂化学键吸收的热量,即c代表反应热;
故答案为:a1 mol H2分裂为H、0.5 mol O2分裂为O时吸收的热量;H、O结合生成1 mol H2O(g)放出的热量;1 mol H2和0.5 mol O2生成1 mol H2O(g)时,反应放出的热量;
②反应物的能量高于生成物的能量,依据化学反应的能量守恒,反应是放热反应,焓变小于0,故答案为:放热;<;
(2)氢气在氧气中可以燃烧可以放出大量的热,氢气的燃烧产物是水,不污染环境,故答案为:放热量高;无污染;
(3)已知:①2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ?mol-1
②H2(g)═H2(l)△H=-0.92kJ?mol-1
③O2(g)═O2(l)△H=-6.84kJ?mol-1
④H2O(l)═H2O(g)△H=+44.0kJ?mol-1
据盖斯定律,①-②×2-③+④×2得:2H2(l)+O2(l)=2H2O(g)△H=-191.12KJ/mol,
故答案为:2H2(l)+O2(l)=2H2O(g)△H=-191.12KJ/mol.
故答案为:a1 mol H2分裂为H、0.5 mol O2分裂为O时吸收的热量;H、O结合生成1 mol H2O(g)放出的热量;1 mol H2和0.5 mol O2生成1 mol H2O(g)时,反应放出的热量;
②反应物的能量高于生成物的能量,依据化学反应的能量守恒,反应是放热反应,焓变小于0,故答案为:放热;<;
(2)氢气在氧气中可以燃烧可以放出大量的热,氢气的燃烧产物是水,不污染环境,故答案为:放热量高;无污染;
(3)已知:①2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ?mol-1
②H2(g)═H2(l)△H=-0.92kJ?mol-1
③O2(g)═O2(l)△H=-6.84kJ?mol-1
④H2O(l)═H2O(g)△H=+44.0kJ?mol-1
据盖斯定律,①-②×2-③+④×2得:2H2(l)+O2(l)=2H2O(g)△H=-191.12KJ/mol,
故答案为:2H2(l)+O2(l)=2H2O(g)△H=-191.12KJ/mol.
点评:本题考查了反应的热量变化的依据和含义、盖斯定律的应用,图象分析、反应实质、能量守恒是解题关键,题目难度中等.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
用铂电极电解CuCl2与CuSO4的混合溶液(浓度均为2mol/L)50mL,当阴极析出9.6g固体时,标准状况下阳极得到的气体是( )
| A、2.24L | B、2.8L |
| C、3.36L | D、4.48L |
尿酸是人体的一种代谢产物,关节炎形成的原因就是在关节的滑液中形成尿酸钠(通常用NaUr表示)晶体:
HUr+H2O?Ur -+H3O+①Ur -+Na+?NaUr②第一次关节炎发作的时间大都在寒冷季节,发病部位常常是手指的关节处,下列推测正确的是( )
HUr+H2O?Ur -+H3O+①Ur -+Na+?NaUr②第一次关节炎发作的时间大都在寒冷季节,发病部位常常是手指的关节处,下列推测正确的是( )
| A、反应②是吸热反应 |
| B、热敷可以使关节炎的症状减轻有一定的道理 |
| C、NaUr易溶于水 |
| D、关节炎发病时关节滑液的pH降低 |
下列实验操作中,主要不是从安全因素考虑的是( )
| A、点燃氢气前一定要检验氢气的纯度 |
| B、未使用完的白磷要随时收集起来,并与空气隔绝 |
| C、用氢气还原氧化铜时,要先通一会儿氢气,再加热氧化铜 |
| D、酒精灯不用时,必须盖上灯帽 |
已知反应:2CO(g)=2C(s)+O2(g).设△H和△S不随温度而变,下列说法中正确的是( )
| A、低温下是自发反应 |
| B、高温下是自发反应 |
| C、低温下是非自发反应,高温下是自发反应 |
| D、任何温度下都是非自发反应 |
下列物质的水溶液由于水解而呈碱性的是( )
| A、NaHSO4 |
| B、NaCl |
| C、Na2CO3 |
| D、NH3 |
某元素的一种同位素X原子的质量数为A,含N个中子,它与1H原子组成HmX分子,在agHmX分子中含质子的物质的量是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
 2NaIO3+5NaHSO3═3NaHSO4+2Na2SO4+I2+H2O.
2NaIO3+5NaHSO3═3NaHSO4+2Na2SO4+I2+H2O.


