题目内容
14.在盛有硝酸银溶液的烧杯中放人用导线连接的铜片和银片,下列叙述正确的是( )| A. | 正极质量不变 | B. | 电流通过导线由铜片流向银片 | ||
| C. | 烧杯中Ag+浓度逐渐减小 | D. | 电池工作时,铜片失电子,被还原 |
分析 Cu、Ag和硝酸银溶液构成原电池,Cu易失电子作负极、Ag作正极,负极上电极反应式为Cu-2e-=Cu 2+、正极反应式为Ag++e-=Ag,电子从负极沿导线流向正极,电流方向与电子流向相反,据此分析解答.
解答 解:Cu、Ag和硝酸银溶液构成原电池,Cu易失电子作负极、Ag作正极,负极上电极反应式为Cu-2e-=Cu 2+、正极反应式为Ag++e-=Ag,电子从负极沿导线流向正极,电流方向与电子流向相反,
A.正极上有Ag析出,所以正极质量增加,故A错误;
B.电子从负极Cu沿导线流向正极Ag,则电流通过导线从Ag流向Cu,故B错误;
C.电池反应式为Cu+2Ag+=2Ag+Cu 2+,所以溶液中Ag+浓度逐渐减小,故C正确;
D.电池工作时,Cu失电子被氧化,故D错误;
故选C.
点评 本题考查原电池原理,为高频考点,明确原电池中正负极判断、电极反应式的书写、电流流向及反应类型是解本题关键,题目难度不大.

| A. | 氨气可用于制造氮肥 | B. | 氯气可用于消毒和制造漂白粉 | ||
| C. | 蔗糖可以食用 | D. | 用工业酒精勾兑的白酒可以饮用 |
| A. | 乙烯的结构简式为CH2CH2 | B. | 羟基的电子式: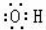 | ||
| C. | Ca2+的结构示意图为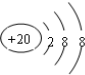 | D. | 乙醇的分子式:CH3CH2OH |
| A. | 常温下,0.5mo1•L-1Fe2(SO4)3溶液中含Fe3+数目为1NA | |
| B. | 标准状况下,22.4L苯中含C-H数目为6NA | |
| C. | 常温常压下,16gO2和O3混合气体中,含氧原子的总数为1NA | |
| D. | 5.6gFe与足量稀盐酸反应,转移电子数为0.3NA |
| 成分的质量/g | 摩尔质量/(g•mol-1?) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.02 | 170 |
(1)下列“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为__________mol•L-1(要求:用原始数据写出表达式即可,不需要化简与计算)。
(2)配制上述“鲜花保鲜剂”所需的仪器有烧杯、玻璃棒、药匙、托盘天平(带砝码)、
____________________(填所缺仪器的名称)。
(3)在溶液配制过程中,下列操作对配制结果没有影响的是_________(填字母).
A.定容时,俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)若要配制0.5mol·L-1500ml的硫酸溶液,则:
①所需质量分数为98%、密度为1.84g·cm-3的浓硫酸的体积为___________(计算结果保留一位小数)mL;
②如果实验室有15mL、20mL、50mL量筒,应选用___________mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸稀释,稀释时操作方法是_____________________.
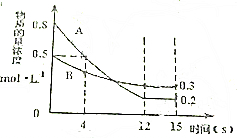 已知:反应aA(g)+bB(g)?cC(g)某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示.
已知:反应aA(g)+bB(g)?cC(g)某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示. 、NO3-、SO42- D.H+、Na+、HCO3-、NO3-
、NO3-、SO42- D.H+、Na+、HCO3-、NO3-