题目内容
工业上可以石油或淀粉为原料生产乙醇.
(1)以石油为原料生产乙醇的一系列反应如图1所示:步骤①称为 ,步骤②称为 .选择一种合适的试剂,完成反应的化学方程式: .
(2)以淀粉为原料生产乙醇,需经过水解、发酵等过程.淀粉水解反应的化学方程式为 (有机物也用化学式表示),每162g淀粉经水解、发酵最终可获得2mol乙醇和另一种无机物,该无机物是 (填化学式).
(3)乙醇跟乙酸在浓硫酸存在并加热的条件下发生酯化反应(反应A),其逆反应是水解反应(反应B).反应可能经历了生成中间体(Ⅰ),过程如图2所示.在A~F 6个反应中,属于加成反应的是 (填字母).
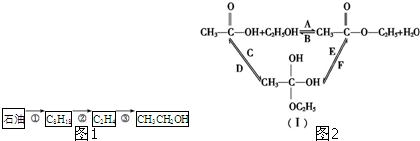
(1)以石油为原料生产乙醇的一系列反应如图1所示:步骤①称为
(2)以淀粉为原料生产乙醇,需经过水解、发酵等过程.淀粉水解反应的化学方程式为
(3)乙醇跟乙酸在浓硫酸存在并加热的条件下发生酯化反应(反应A),其逆反应是水解反应(反应B).反应可能经历了生成中间体(Ⅰ),过程如图2所示.在A~F 6个反应中,属于加成反应的是

考点:淀粉的性质和用途,取代反应与加成反应,石油的裂化和裂解,石油的分馏
专题:
分析:(1)依据石油炼制的原理结合乙烯的化学性质解答;
(2)淀粉为多糖,水解生成最终产物为葡萄糖;依据原子个数守恒判断无机物成分;
(3)取代反应:“有机化合物分子里的某些原子或原子团被其它原子或原子团所代替的反应”特点是:有去有回;
加成反应指:有机物中的不饱和键被加成试剂原子加成为饱和键的反应,加成反应特点是:有去无回;
消去反应指:有机物中脱去一个或几个小分子(如水、卤化氢等分子),而生成不饱和(碳碳双键或三键或苯环状)化合物的反应;特点是:生成不饱和化合物;
据此解答.
(2)淀粉为多糖,水解生成最终产物为葡萄糖;依据原子个数守恒判断无机物成分;
(3)取代反应:“有机化合物分子里的某些原子或原子团被其它原子或原子团所代替的反应”特点是:有去有回;
加成反应指:有机物中的不饱和键被加成试剂原子加成为饱和键的反应,加成反应特点是:有去无回;
消去反应指:有机物中脱去一个或几个小分子(如水、卤化氢等分子),而生成不饱和(碳碳双键或三键或苯环状)化合物的反应;特点是:生成不饱和化合物;
据此解答.
解答:
解:(1)石油是含有不同沸点的混合物,通过石油的分馏将石油成不同沸点短产物,然后通过石油的裂化或者裂解将大分子的烃断裂为小分子烃,乙烯与水在一定条件下反应生成乙醇,方程式为:C2H4+H2O
CH3CH2OH;
故答案为:分馏;裂化或裂解;C2H4+H2O
CH3CH2OH;
(2)淀粉为多糖,水解生成最终产物为葡萄糖,化学方程式为( C6H10O5)n+nH2O
nC6H12O6;
依据方程式可知:每162g淀粉经水解、发酵最终可获得2mol乙醇和另一种无机物,依据质量守恒:162+18=2×46+m,解得m=88g,依据原子个数守恒可知该无机物含有C和O两种元素,所以为二氧化碳;
故答案为:( C6H10O5)n+nH2O
nC6H12O6;CO2;
(3)A反应,乙酸中的羟基被CH3CH2O-取代生成乙酸乙酯,该反应属于取代反应;
B中乙酸乙酯水解为A的逆反应,属于取代反应;
C反应,乙酸中碳氧双键打开,与乙醇发生加成,属于加成反应;
E中,乙酸乙酯和水发生加成反应;
F中,一种物质生成两种物质,属于消去反应;
D反应产物乙酸中含有碳氧双键,E反应中生成乙酸乙酯中含有碳氧双键,所以这两反应属于消去反应;
故选:CE.
| 一定条件 |
故答案为:分馏;裂化或裂解;C2H4+H2O
| 一定条件 |
(2)淀粉为多糖,水解生成最终产物为葡萄糖,化学方程式为( C6H10O5)n+nH2O
| 一定条件 |
依据方程式可知:每162g淀粉经水解、发酵最终可获得2mol乙醇和另一种无机物,依据质量守恒:162+18=2×46+m,解得m=88g,依据原子个数守恒可知该无机物含有C和O两种元素,所以为二氧化碳;
故答案为:( C6H10O5)n+nH2O
| 一定条件 |
(3)A反应,乙酸中的羟基被CH3CH2O-取代生成乙酸乙酯,该反应属于取代反应;
B中乙酸乙酯水解为A的逆反应,属于取代反应;
C反应,乙酸中碳氧双键打开,与乙醇发生加成,属于加成反应;
E中,乙酸乙酯和水发生加成反应;
F中,一种物质生成两种物质,属于消去反应;
D反应产物乙酸中含有碳氧双键,E反应中生成乙酸乙酯中含有碳氧双键,所以这两反应属于消去反应;
故选:CE.
点评:本题考查了有机物的结构与性质及反应类型的判断,熟悉淀粉的结构与性质、熟悉石油炼制的过程和原理是解题关键,注意有机反应的类型及特点,题目难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式正确的是( )
| A、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| B、醋酸与NaHCO3溶液反应:H++HCO3-=CO2↑+H2O |
| C、将少量铜屑放入浓硝酸中的反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| D、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
2012年10月24日飓风“桑迪”袭击美国.一阵飓风过后,海面的巨浪上竟燃烧着熊熊大火.海水会燃烧的原因是( )
| A、飓风与海水发生剧烈摩擦,产生的巨大热能使水分子分解,引起氢气燃烧 |
| B、飓风使海水温度升高,产生高温水蒸气,达到水的着火点,使海水燃烧 |
| C、飓风产生高温,使氮气在空气中剧烈燃烧 |
| D、以上说法均有可能 |
下列说法正确的是( )
| A、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| B、重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 |
| C、在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液 |
| D、Cl-、S2-、Ca2+、K+半径逐渐减小 |
某同学欲检验淀粉水解的情况,设计了下列实验,A、B、C、D都是实验室常用的无机试剂.则A、B、C、D分别是( )
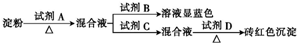

| A、稀硫酸、碘水、NaOH溶液、新制氢氧化铜 |
| B、稀硫酸、碘水、稀硫酸、CuSO4溶液 |
| C、NaOH溶液、碘水、稀硫酸、新制氢氧化铜 |
| D、稀硫酸、KI溶液、NaOH溶液、新制氢氧化铜 |
NA表示阿伏加德罗常数,以下说法中正确的是( )
| A、2.3 g钠由原子变为离子时失去的电子数为NA |
| B、在常温常压下,1 mol氩气含有的原子数为2NA |
| C、标准状况下2.24 L氨气所含电子总数为0.1NA |
| D、在常温常压下,62 g Na2O中含有O2-离子数为NA |




