题目内容
16.在给定的条件下,下列选项所示的物质间转化均能一步实现的是( )| A. | Na$→_{点燃}^{O_{2}}$Na2O2$\stackrel{CO_{2}}{→}$Na2CO3 | B. | FeS2$→_{煅烧}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | ||
| C. | NaCl(aq)$\stackrel{电解}{→}$Cl2$→_{△}^{过量Fe}$FeCl2(s) | D. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3 |
分析 A、钠在氧气中燃烧生成淡黄色的过氧化钠,过氧化钠与二氧化碳反应生成碳酸钠和氧气;
B、二硫化亚铁在氧气中煅烧生成二氧化硫;
C、电解氯化钠的水溶液生成氯气,铁与氯气反应生成氯化铁;
D、二氧化硅不溶于水,也不与水反应.
解答 解:A、钠在氧气中燃烧生成淡黄色的过氧化钠,过氧化钠与二氧化碳反应生成碳酸钠和氧气,所以能实现Na$→_{点燃}^{O_{2}}$Na2O2$\stackrel{CO_{2}}{→}$Na2CO3,各步转化,故A正确;
B、二硫化亚铁在氧气中煅烧生成二氧化硫,而不是三氧化硫,故B错误;
C、电解氯化钠的水溶液生成氯气,铁与氯气反应生成氯化铁,而不是氯化亚铁,故C错误;
D、二氧化硅不溶于水,也不与水反应,所以不能实现,故D错误;
故选A.
点评 本题考查了物质性质的分析应用,主要是反应产物和反应条件的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
11.下列化学用语正确的是( )
| A. | NaCl的电子式: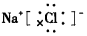 | B. | 硫离子的结构示意图: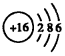 | ||
| C. | 氮气的结构式::N≡N: | D. | 次氯酸的电子式:H:Cl:O: |
7.有A、B、C、D、E五种原子序数小于18的元素,其特征信息如下表:
请回答下列问题:
(1)A、B、C三种元素形成的化合物含有的化学键类型是离子键、(极性)共价键.
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
(3)D单质与A、E形成的化合物的水溶液反应的离子方程式是2Al+6H+=2Al3++3H2↑.
(4)写出实验室制取单质E的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(5)C和D两元素形成的单质活泼性较强的是(写元素符号)Na,你的判断依据是Na可与冷水剧烈反应,Al不与水反应.
| 元素编号 | 特征信息 |
| A | 有一种原子内只有质子,没有中子 |
| B | L层电子数是K层的3倍 |
| C | 其阳离子与B的阴离子具有相同的电子层结构,且核电荷数与B相差3 |
| D | 最外层电子数等于电子层数,且是地壳中含量较多的元素之一 |
| E | 单质为黄绿色,可用于制造漂白粉 |
(1)A、B、C三种元素形成的化合物含有的化学键类型是离子键、(极性)共价键.
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
(3)D单质与A、E形成的化合物的水溶液反应的离子方程式是2Al+6H+=2Al3++3H2↑.
(4)写出实验室制取单质E的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(5)C和D两元素形成的单质活泼性较强的是(写元素符号)Na,你的判断依据是Na可与冷水剧烈反应,Al不与水反应.
4.短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的最高正价与最低负价的代数和为2,Y是地壳中含量最多的元素,Z原子的最外层电子数是Y原子的最外层电子数的一半,W与Y同主族.下列说法正确的是( )
| A. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| B. | 元素X、Y组成的化合物只有两种 | |
| C. | W的简单气态氢化物的热稳定性比Y的弱 | |
| D. | Q、Z的简单离子具有相同的电子层结构 |
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 500mL0.l mol/LFeCl3溶液中含Fe3+0.05NA | |
| B. | 常温常压下,2.24L氯气溶于NaOH溶液中,转移电子数为0.lNA | |
| C. | 常温常压下,28g乙烯中所含C-H键的数目为4NA | |
| D. | 0.5 mol锌与浓硫酸完全反应生成SO2和H2的混合气体(不考虑气体溶解),气体的分子总数小于0.5NA |
1.常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为离子晶体;
(2)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如表所示:
则元素Y第一电离能大于X的原因是Mg为3s2构型,完全充满状态,是一种稳定结构;
(3)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损.铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成配合物黄血盐.
①写出亚铁离子的核外电子排布式[Ar]3d6;
②1mol CN-中π键数目为2NA .
(1)“氯盐类”融雪剂主要成分的晶体类型为离子晶体;
(2)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
(3)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损.铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成配合物黄血盐.
①写出亚铁离子的核外电子排布式[Ar]3d6;
②1mol CN-中π键数目为2NA .
8.利用如图所示的装置可将CO2转化为燃料甲醇,下列说法正确的是( )


| A. | b极发生还原反应 | |
| B. | a极的电极反应:CH3OH+H2O-6e-═CO2+6H+ | |
| C. | 总反应方程式为:2CO2+4H2O$\frac{\underline{\;通电\;}}{\;}$2CH3OH+3O2 | |
| D. | 该装置将化学能转变为电能 |
5.能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H;下表所列数据是该反应在不同温度下的化学平衡常数(K).
①写出该反应的平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{c(CO)•{c}^{2}({H}_{2})}$.
②下列措施可以加快反应速率且能提高CO转化率的是c.
a.再充入CO b.将甲醇液化并及时分离出c.增大压强 d.加入催化剂 e.降低温度
③在300℃时,将2molCO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将向正反应方向进行 (填“向正反应方向进行”“向逆反应方向进行”或“处于平衡状态”).
(2)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4OH-=2CO32-+6H2O,则负极的电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O.
(3)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为:2Cl--2e-=Cl2↑;如果电解一段时间后NaC1溶液的体积为1L,溶液中的OH-物质的量浓度为0.01mol•L-1(25℃下测定),则理论上消耗氧气的体积为56mL(标况下).
(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H;下表所列数据是该反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②下列措施可以加快反应速率且能提高CO转化率的是c.
a.再充入CO b.将甲醇液化并及时分离出c.增大压强 d.加入催化剂 e.降低温度
③在300℃时,将2molCO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将向正反应方向进行 (填“向正反应方向进行”“向逆反应方向进行”或“处于平衡状态”).
(2)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4OH-=2CO32-+6H2O,则负极的电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O.
(3)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为:2Cl--2e-=Cl2↑;如果电解一段时间后NaC1溶液的体积为1L,溶液中的OH-物质的量浓度为0.01mol•L-1(25℃下测定),则理论上消耗氧气的体积为56mL(标况下).
18.化学与我们的生活息息相关,下列有关说法正确的是( )
| A. | SO2、NO2都是酸性氧化物,分别能形成硫酸型酸雨和硝酸型酸雨 | |
| B. | 明矾[KAl(SO4)2•l2H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 | |
| C. | 高铁车厢大部分材料是铝合金,铝合金材料具有强度大、质量轻、抗腐蚀能力强等优点 | |
| D. | 日常生活中常用汽油去除衣物上的油污,用热的纯碱溶液洗涤炊具上的油污,两者的原理完全相同 |