题目内容
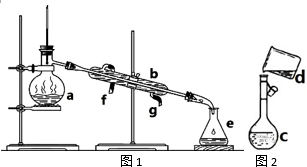 掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置.(1)写出下列仪器的名称:a.
(2)仪器a~e中,使用前必须检查是否漏水的有
(3)若利用图1所示装置分离四氯化碳和酒精的混合物,还缺少的仪器是
(4)现需配制0.1mol?L-1NaOH溶液450mL,图2中装置是某同学转移溶液的示意图.
①图中的错误是
②根据计算得知,所需NaOH的质量为
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶;
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解;
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中;
D.将容量瓶盖紧,振荡,摇匀;
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切;
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处.
④配制0.1mol?L-1NaOH溶液的实验中,如果出现以下操作:
A.称量时用了生锈的砝码
B.将NaOH放在纸张上称量
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.定容时仰视刻度线
E.容量瓶未干燥即用来配制溶液
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
上述操作中对配制的溶液物质的量浓度大小造成(填写字母)偏大的有
考点:蒸馏与分馏
专题:实验题
分析:(1)根据仪器的结构特点判断;
(2)容量瓶在使用前一定要查漏;
(3)分离四氯化碳和酒精的混合物,根据沸点不同分离,即用分馏的方法,分馏需要酒精灯加热;
(4)①根据配制一定物质的量浓度的溶液的方法和操作来寻找装置中的错误;根据配制溶液的实验操作过程选择所用仪器;
②先依据常见容量瓶的规格及所配溶液的体积选择合适的容量瓶,然后根据m=nM=cvM计算所需氢氧化钠的质量;
③根据操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作步骤确定顺序;
④根据c=
分析操作对溶质的物质的量或对溶液的体积的影响判断.
(2)容量瓶在使用前一定要查漏;
(3)分离四氯化碳和酒精的混合物,根据沸点不同分离,即用分馏的方法,分馏需要酒精灯加热;
(4)①根据配制一定物质的量浓度的溶液的方法和操作来寻找装置中的错误;根据配制溶液的实验操作过程选择所用仪器;
②先依据常见容量瓶的规格及所配溶液的体积选择合适的容量瓶,然后根据m=nM=cvM计算所需氢氧化钠的质量;
③根据操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作步骤确定顺序;
④根据c=
| n |
| V |
解答:
解:(1)a为蒸馏烧瓶,b为冷凝管,c为容量瓶,故答案为:蒸馏烧瓶;冷凝管;容量瓶;
故答案为:蒸馏烧瓶;冷凝管;容量瓶;
(2)容量瓶在使用前一定要查漏,故答案为:c;
(3)分离四氯化碳和酒精的混合物,根据沸点不同分离,即用分馏的方法,分馏需要酒精灯加热;
故答案为:酒精灯;
(3)①配制一定物质的量浓度的溶液是必须用玻璃棒引流,防止液体外溅;
②没有450mL规格容量瓶,所以选用500mL容量瓶,操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙;
故答案为:没有用玻璃棒引流;玻璃棒 胶头滴管,药匙;
②没有450mL规格容量瓶,所以选用500mL容量瓶,需氢氧化钠的质量为m=0.5L×0.1mol?L-1×40g/mol=2.0g;
故答案为:2.0g;
③配制溶液500mL,配制步骤有称量、溶解、移液、洗涤、移液、定容、摇匀等操作,用托盘天平称量2.0gNaOH,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤,并将洗涤液移入容量瓶,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液凹液面的最低点与刻度线相切,最后定容颠倒摇匀,所以操作顺序为BCAFED;
故答案为:BCAFED;
④A.称量时用了生锈的砝码,称取的氢氧化钠质量偏大,n偏大,浓度偏大,故A正确;
B.将NaOH放在纸张上称量,氢氧化钠吸收空气中的水分和二氧化碳,称取的氢氧化钠质量偏小,n偏小,浓度偏小,故B错误;
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,冷却后溶液体积不到500ml,V偏小,浓度偏大,故C正确;
D.定容时仰视刻度线,溶液的体积偏大,浓度偏小,故D错误;
E.容量瓶未干燥即用来配制溶液,没有影响,故E错误;
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,所配溶液体积V偏大,浓度偏小,故F错误;
故答案为:AC.
故答案为:蒸馏烧瓶;冷凝管;容量瓶;
(2)容量瓶在使用前一定要查漏,故答案为:c;
(3)分离四氯化碳和酒精的混合物,根据沸点不同分离,即用分馏的方法,分馏需要酒精灯加热;
故答案为:酒精灯;
(3)①配制一定物质的量浓度的溶液是必须用玻璃棒引流,防止液体外溅;
②没有450mL规格容量瓶,所以选用500mL容量瓶,操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙;
故答案为:没有用玻璃棒引流;玻璃棒 胶头滴管,药匙;
②没有450mL规格容量瓶,所以选用500mL容量瓶,需氢氧化钠的质量为m=0.5L×0.1mol?L-1×40g/mol=2.0g;
故答案为:2.0g;
③配制溶液500mL,配制步骤有称量、溶解、移液、洗涤、移液、定容、摇匀等操作,用托盘天平称量2.0gNaOH,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤,并将洗涤液移入容量瓶,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液凹液面的最低点与刻度线相切,最后定容颠倒摇匀,所以操作顺序为BCAFED;
故答案为:BCAFED;
④A.称量时用了生锈的砝码,称取的氢氧化钠质量偏大,n偏大,浓度偏大,故A正确;
B.将NaOH放在纸张上称量,氢氧化钠吸收空气中的水分和二氧化碳,称取的氢氧化钠质量偏小,n偏小,浓度偏小,故B错误;
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,冷却后溶液体积不到500ml,V偏小,浓度偏大,故C正确;
D.定容时仰视刻度线,溶液的体积偏大,浓度偏小,故D错误;
E.容量瓶未干燥即用来配制溶液,没有影响,故E错误;
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,所配溶液体积V偏大,浓度偏小,故F错误;
故答案为:AC.
点评:本题考查学生化学实验的基本操作知识,可以根据所学知识来回答,注意配制450mL溶液需要选用500mL容量瓶,本题难度不大.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
A、澄清石灰水与过量NaHCO3溶液混合:Ca2++OH-+HCO
| ||
B、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO
| ||
| C、锌和稀硝酸的反应:Zn2++2H+=Zn2++H2 | ||
| D、CuSO4溶液吸收H2S气体:Cu2++H2S=CuS↓+2H+ |
下列氧化还原反应中,实际参加反应的氧化剂与还原剂物质的量之比正确的是( )
①2H2S+SO2=3S+2H2O; 1:2
②6HNO3(浓)+S=H2SO4+6NO2+2H2O; 6:1
③Fe+4HNO3=Fe(NO3)3+NO+2H2O; 1:1
④2Na2O2+2H2O=4NaOH+O2; 1:1.
①2H2S+SO2=3S+2H2O; 1:2
②6HNO3(浓)+S=H2SO4+6NO2+2H2O; 6:1
③Fe+4HNO3=Fe(NO3)3+NO+2H2O; 1:1
④2Na2O2+2H2O=4NaOH+O2; 1:1.
| A、只有①正确 |
| B、只有③ |
| C、只有①和④ |
| D、①②③④都正确 |
下列热化学方程式或离子方程式中,正确的是( )
| A、从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| B、向Mg(HCO3)2溶液中加入过量的澄清石灰水:Mg2++2HCO3-+2OH一+Ca2+═MgCO3↓+CaCO3↓+2H2O |
| C、乙烯的燃烧热为akJ/mol(a>0),则乙烯燃烧的热化学方程式可表示为:C2H4(g)+3O2(g)═2CO2(g)+2H2O(g)△H=-akJ/mol |
| D、Ba(OH)2溶液中加入过量的Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
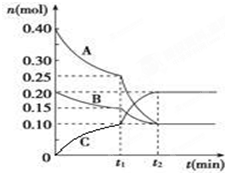 现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图:
现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图: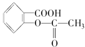 ,作为一种解热镇痛药,对于感冒发烧,它有较好的疗效,但大剂量长期空腹服用,容易对胃肠道产生刺激,原因是阿司匹林在胃中会发生酯的水解反应,生成(用结构简式表示)
,作为一种解热镇痛药,对于感冒发烧,它有较好的疗效,但大剂量长期空腹服用,容易对胃肠道产生刺激,原因是阿司匹林在胃中会发生酯的水解反应,生成(用结构简式表示)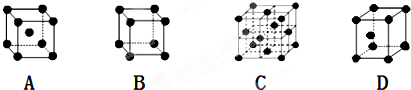
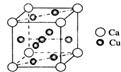 是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为
是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为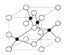 是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为
是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为