题目内容
4.化学与生活、生产、国防、科技等方面密切相关,下列有关说法错误的是( )| A. | 用灼烧的方法可以区分羊毛和人造纤维 | |
| B. | 医用消毒酒精是体积分数为95%的乙醇 | |
| C. | 食用一定量的油脂能促进人体对某些维生素的吸收 | |
| D. | 加热能杀死流感病毒是因为蛋白质受热变性 |
分析 A.羊毛的主要成分是蛋白质,具有蛋白质的性质;
B.75%的酒精对细菌蛋白质的渗透效果最好;
C.食用的油脂供给脂溶性维生素作溶剂;
D.蛋白质受热易变性.
解答 解:A.羊毛的主要成分是蛋白质,具有蛋白质的性质,灼烧时具有烧焦羽毛的气味,人造纤维灼烧没有烧焦羽毛的气味,所以用灼烧的方法区分羊毛和人造纤维,故A正确;
B.75%的酒精对细菌蛋白质的渗透效果最好,为医用酒精,故B错误;
C.油脂既能运送营养素,也能作为维生素A、D、E、K的溶剂,它们必须溶在油脂里面,才会被消化吸收,故C正确;
D.蛋白质受热变性而失去活性,所以加热能杀死流感病毒是因为蛋白质受热变性,故D正确;
故选B.
点评 本题考查化学与生活,为高频考点,明确元素化合物性质是解本题关键,会运用化学知识解释生产生活知识,题目难度不大.

练习册系列答案
相关题目
14.Ⅰ.已知:Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如表系列实验:
(1)该实验①、②可探究温度对反应速率的影响,因此V1=10.0,V2=10.0,V3=0.
(2)下列有关该实验的叙述正确的是A(填字母).
A.实验前,应先用黑墨水笔在白纸上画粗浅一致的“+”字,衬在锥形瓶底部,实验中记录反应开始到产生的浑浊将锥形瓶底部的“+”字刚好完全遮盖所需的时间
B.该实验所需的计量仪器有量筒、温度计
C.实验时,应先将量取的Na2S2O3和H2SO4溶液混合,然后置于相应温度的热水浴中反应,记录每组反应所需时间
(3)实验过程中为什么不用测量一定时间内放出SO2气体的量来表示该反应的化学反应速率的大小?SO2易溶于水,无法准确测量其体积.
Ⅱ.已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如图2所示.
(4)25.0℃时,0~6min氨基甲酸铵水解反应的平均速率为0.05mol/(L•min).
(5)根据图中信息,如何说明该水解反应的速率随温度升高而增大:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
| 实验 序号 | 反应温 度/℃ | Na2S2O3溶液 | 稀硫酸 | H2O | ||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(2)下列有关该实验的叙述正确的是A(填字母).
A.实验前,应先用黑墨水笔在白纸上画粗浅一致的“+”字,衬在锥形瓶底部,实验中记录反应开始到产生的浑浊将锥形瓶底部的“+”字刚好完全遮盖所需的时间
B.该实验所需的计量仪器有量筒、温度计
C.实验时,应先将量取的Na2S2O3和H2SO4溶液混合,然后置于相应温度的热水浴中反应,记录每组反应所需时间
(3)实验过程中为什么不用测量一定时间内放出SO2气体的量来表示该反应的化学反应速率的大小?SO2易溶于水,无法准确测量其体积.
Ⅱ.已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如图2所示.
(4)25.0℃时,0~6min氨基甲酸铵水解反应的平均速率为0.05mol/(L•min).
(5)根据图中信息,如何说明该水解反应的速率随温度升高而增大:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
15.化学在生产和日常生活中有着重要的作用,下列说法错误的是( )
| A. | 即将发射的嫦娥五号卫星使用的碳纤维是一种新型无机非金属材料 | |
| B. | 我国古代闻名于世界的化学工艺有烧陶瓷、造纸、冶金、制火药等 | |
| C. | 夏天雷雨过后感觉到空气清新是因为空气中产生了少量的氮氧化物 | |
| D. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 |
12.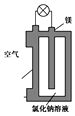 镁与锂相比有多种优点,比如锂的熔点约为180摄氏度,而镁的熔点高达约650摄氏度,因而更为安全,镁的蕴藏量也比锂丰富得多.图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料.下列有关该镁燃料电池的叙述正确的是( )
镁与锂相比有多种优点,比如锂的熔点约为180摄氏度,而镁的熔点高达约650摄氏度,因而更为安全,镁的蕴藏量也比锂丰富得多.图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料.下列有关该镁燃料电池的叙述正确的是( )
 镁与锂相比有多种优点,比如锂的熔点约为180摄氏度,而镁的熔点高达约650摄氏度,因而更为安全,镁的蕴藏量也比锂丰富得多.图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料.下列有关该镁燃料电池的叙述正确的是( )
镁与锂相比有多种优点,比如锂的熔点约为180摄氏度,而镁的熔点高达约650摄氏度,因而更为安全,镁的蕴藏量也比锂丰富得多.图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料.下列有关该镁燃料电池的叙述正确的是( )| A. | 圆筒为正极,电极反应式为O2+4e-═2O2- | |
| B. | 该电池的总反应为2Mg+O2+2H2O═2Mg(OH)2 | |
| C. | Cl-在阳极失去电子生成Cl2 | |
| D. | 在反应过程中消耗24g的镁,同时消耗空气的体积大约为11.2L(标准状况) |
19.化学与生产、生活、社会发展息息相关.下列说法正确的是( )
| A. | 食品包装时放入盛有还原铁粉的透气小袋可防止食品氧化变质 | |
| B. | 聚乙烯、聚氯乙烯均可作为包装材料,且不会造成环境污染 | |
| C. | 华为自主研发的“麒麟”芯片与光导纤维是同种材料 | |
| D. | 小苏打能作焙制蛋糕的膨松剂是由于小苏打能与碱反应生成CO2 |
9.图象常作为描述化学过程的一种方法,在化学中大量运用.下列有关图象的说法正确的是( )
| A. | 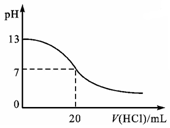 表示V L 0.1mol/L的氨水中滴加某种浓度的盐酸时,溶液pH的变化情况 | |
| B. | 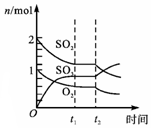 表示SO2与O2的可逆反应,t2时刻条件的改变可能是压强 | |
| C. | 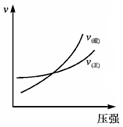 表示一个气体总休积减小的可逆反应中,压强与反应速率的关系 | |
| D. | 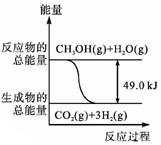 表示某种放热反应,反应热为49.0kJ |
16.设NA为阿伏伽德罗常数的值,下列说法正确的是标( )
| A. | 标准状况下,2.24L乙醇中碳氢键的数目为0.5NA | |
| B. | 1L0.1mol•L-1硫酸钠溶液中含有的氧原子数为0.4NA | |
| C. | 0.1molKI与0.1molFeCl3在溶液中反应转移的电子数为0.1NA | |
| D. | 0.1mol乙稀与乙醇的混合物完全燃烧所消耗的氧分子数为0.3NA |
7.下列实验操作中,错误的是( )
| A. | 现需80 mL 1.0 mol•L-1 NaOH溶液,称取3.2 g NaOH固体配制溶液浓度偏小 | |
| B. | 装标准液的滴定管未润洗,测得待测液的浓度偏大 | |
| C. | 用pH试纸测得新制氯水的pH为2 | |
| D. | 用酸式滴定管准确量取10.00mLKMnO4溶液 |
8.下列各项中的两组反应都是在溶液中进行的,它们不能用同一离子方程式表示的是( )
| A. | HCl+Zn,Zn+NaHSO4 | B. | Cu(OH)2+H2SO4,Cu(OH)2+HNO3 | ||
| C. | CaO+HCl,CaO+HNO3 | D. | BaCl2+NaHSO4,Ba(OH)2+NaHSO4(少量) |