题目内容
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池.电池的总反应为:CH4+2O2+2KOH=K2CO3+3H2O则下列说法正确的是( )
①通入甲烷的电极为电池的正极,
②通入氧气的电极为正极
③每有1molCH4被氧化,转移8mol电子
④电池放电后,溶液PH不断升高.
①通入甲烷的电极为电池的正极,
②通入氧气的电极为正极
③每有1molCH4被氧化,转移8mol电子
④电池放电后,溶液PH不断升高.
| A、①② | B、②③ | C、①④ | D、③④ |
考点:原电池和电解池的工作原理
专题:
分析:碱性CH4燃料电池,具有还原性的甲烷为原电池的负极,发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O,通入氧气的一极为原电池的正极,发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,原电池工作时,电子从负极经外电路流向正极,电解质溶液中,阳离子向正极移动,阴离子向负极移动,据此分析.
解答:
解:①燃料电池中,燃料甲烷在负极是典型的发生氧化反应,氧气在正极得到电子发生还原反应,故①错误;
②燃料电池中,燃料甲烷在负极是典型的发生氧化反应,氧气在正极得到电子发生还原反应,故②正确;
③通入CH4的电极为负极失电子反应氧化反应,电极反应为:CH4+10OH--8e-=CO32-+7H2O,1molCH4被氧化,转移8mol电子,故③正确;
④电池反应式为:CH4+2OH-+2O2=CO32-+3H2O,随着反应的进行,溶液中氢氧根离子不断减少,溶液pH不断减小,故④错误;
故选B.
②燃料电池中,燃料甲烷在负极是典型的发生氧化反应,氧气在正极得到电子发生还原反应,故②正确;
③通入CH4的电极为负极失电子反应氧化反应,电极反应为:CH4+10OH--8e-=CO32-+7H2O,1molCH4被氧化,转移8mol电子,故③正确;
④电池反应式为:CH4+2OH-+2O2=CO32-+3H2O,随着反应的进行,溶液中氢氧根离子不断减少,溶液pH不断减小,故④错误;
故选B.
点评:本题考查了燃料电池,电极反应式的书写要注意结合电解质溶液判断电极上的生成物,原料相同,电解质溶液不同,电极反应式就不同;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
A、按系统命名法,化合物 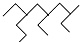 的名称为2,4-二乙基-6-丙基辛烷 的名称为2,4-二乙基-6-丙基辛烷 |
| B、若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
| C、醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物 |
D、1mol某有机物的结构简式为 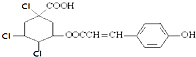 通过消去反应脱去1 molHCl时,能得到 5 种不同产物(不考虑立体异构) 通过消去反应脱去1 molHCl时,能得到 5 种不同产物(不考虑立体异构) |
下列溶液中微粒的物质的量浓度关系正确的是( )
A、常温下电离常数为Ka的酸HA 溶液中 c (H+)=
| ||
| B、0.2mol?L-1 CH3COOH溶液与0.1mol?L-1NaOH溶液等体积混合2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) | ||
| C、将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp(CaSO4) | ||
| D、常温下,向0.1mol/L NH4HSO4溶液中滴加NaOH溶液至中性c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
已知NaHSO3溶液显酸性,溶液中存在以下平衡:HSO3-+H2O?H2SO3+OH-①HSO3-?H++SO32-②,向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
| A、加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | ||||||||
B、加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+
| ||||||||
C、加入少量NaOH溶液,
| ||||||||
| D、加入氨水至中性,则2c(Na+)=c(SO32-)>c(H+)=c(OH-) |
25℃,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A、向水中加入冰醋酸,平衡逆向移动,c(H+)降低 |
| B、向水中加入少量固体碳酸氢钠,c(H+)增大,Kw不变 |
| C、向水中加入少量固体CH3COONa,平衡正向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |
下列物质中只含有离子键的是( )
| A、CaCl2 |
| B、C2H4 |
| C、N2 |
| D、Na202 |




