题目内容
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的
,A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物.请回答下列问题:
(1)C和E两种元素相比较,非金属性较强的是(填元素名称) ,可以验证该结论的是(填写编号) ;
A.比较这两种元素的常见单质的沸点
B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的气态氢化物的酸性
(2)A、C、D、E可形成两种酸式盐(均有四种元素组成),两种酸式盐相互反应的离子方程式为 .
(3)A、C、E间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 .
(4)在火箭推进器中装有液态B2A4和液态A2C2,已知0.4mol液态B2A4和足量液态A2C2反应,生成气态B2和气态A2C,放出256.6kJ的热量.试写出该反应的热化学方程式: .
(5)A、B、C可形成一种18电子的分子,该分子可与盐酸反应生成一种盐.写出该盐的电子式 .
| 3 |
| 4 |
(1)C和E两种元素相比较,非金属性较强的是(填元素名称)
A.比较这两种元素的常见单质的沸点
B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的气态氢化物的酸性
(2)A、C、D、E可形成两种酸式盐(均有四种元素组成),两种酸式盐相互反应的离子方程式为
(3)A、C、E间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(4)在火箭推进器中装有液态B2A4和液态A2C2,已知0.4mol液态B2A4和足量液态A2C2反应,生成气态B2和气态A2C,放出256.6kJ的热量.试写出该反应的热化学方程式:
(5)A、B、C可形成一种18电子的分子,该分子可与盐酸反应生成一种盐.写出该盐的电子式
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D、E五种短周期元素,它们的原子序数依次增大.A元素的原子半径最小,则A为H元素;B元素的最高价氧化物对应的水化物与其氢化物能生成盐,则B为N元素;E元素原子的最外层电子数是其次外层电子数的3/4,则E原子核外有3的电子层,最外层电子数为6,在E为S元素;D与A同主族,且与E同周期,则D为Na元素;A、B、D、E这四种元素都能与C元素形成原子个数比不相同的若干种化合物,则C为氧元素,据此解答各小题即可.
解答:
解:依据分析可知:A为氢,B为氮,C为氧,D为钠,E为硫,
(1)O和S两种元素相比较,非金属性较强的是O,同一主族中,原子序数越小,非金属性越强,可以利用与氢气反应的难易程度、氢化物的稳定性进行验证,不能利用其物理性质判断,水显中性,不能利用其氢化物的酸性比较,故答案为:氧;BC;
(2)H、N、O、S形成两种酸式盐(均由四种元素组成)为NaHSO3、NaHSO4,二者反应的离子方程式为:HSO3-+H+=SO2↑+H2O,故答案为:HSO3-+H+=SO2↑+H2O;
(3)H、O、S间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,甲有18个电子,则甲为HS-,乙有10个电子,则乙为OH-,甲与乙反应的离子方程式为:HS-+OH-=S2-+H2O,
故答案为:HS-+OH-=S2-+H2O;
(4)在火箭推进器中装有液态N2H4和液态H2O2,0.4mol液态N2H4和足量液态H2O2反应,生成气态N2和气态H2O,放出256.6kJ的热量,则1mol液态N2H4反应放出的热量为256.6kJ×
=641.5kJ,故该反应的热化学方程式为:N2H4(l)+2 H2O2(l)=N2(g)+4H2O(g)△H=-641.5kJ?mol-1,
故答案为:N2H4(l)+2 H2O2(l)=N2(g)+4H2O(g)△H=-641.5kJ?mol-1;
(5)H、N、O可形成一种18电子的分子为:NH2OH,该分子可与盐酸反应生成一种盐:[NH3OH]Cl,该盐的电子式为: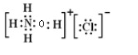 ,
,
故答案为: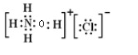 .
.
(1)O和S两种元素相比较,非金属性较强的是O,同一主族中,原子序数越小,非金属性越强,可以利用与氢气反应的难易程度、氢化物的稳定性进行验证,不能利用其物理性质判断,水显中性,不能利用其氢化物的酸性比较,故答案为:氧;BC;
(2)H、N、O、S形成两种酸式盐(均由四种元素组成)为NaHSO3、NaHSO4,二者反应的离子方程式为:HSO3-+H+=SO2↑+H2O,故答案为:HSO3-+H+=SO2↑+H2O;
(3)H、O、S间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,甲有18个电子,则甲为HS-,乙有10个电子,则乙为OH-,甲与乙反应的离子方程式为:HS-+OH-=S2-+H2O,
故答案为:HS-+OH-=S2-+H2O;
(4)在火箭推进器中装有液态N2H4和液态H2O2,0.4mol液态N2H4和足量液态H2O2反应,生成气态N2和气态H2O,放出256.6kJ的热量,则1mol液态N2H4反应放出的热量为256.6kJ×
| 1mol |
| 0.4mol |
故答案为:N2H4(l)+2 H2O2(l)=N2(g)+4H2O(g)△H=-641.5kJ?mol-1;
(5)H、N、O可形成一种18电子的分子为:NH2OH,该分子可与盐酸反应生成一种盐:[NH3OH]Cl,该盐的电子式为:
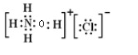 ,
,故答案为:
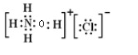 .
.
点评:本题考查元素化合物推断、常用化学用语、元素周期律、热化学方程式的书写等,推断元素是解题关键,侧重对基础知识的巩固利用,难度不大.

练习册系列答案
相关题目
 有X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16.X、Y、Z三种元素的常见单质在适当条件下可发生如下变化,其中B和C均为10电子分子.下列说法中不正确的是( )
有X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16.X、Y、Z三种元素的常见单质在适当条件下可发生如下变化,其中B和C均为10电子分子.下列说法中不正确的是( )| A、X元素位于ⅥA |
| B、热稳定性:B>C |
| C、C极易溶于B中,溶液呈碱性 |
| D、A和C不可能发生氧化还原反应 |
下列说法正确的是( )
| A、用加热法可除去Na2CO3中的NaHCO3 |
| B、Na、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的碱 |
| C、可用石灰水区分Na2CO3与NaHCO3溶液 |
| D、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
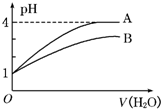 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )| A、A酸比B酸的电离程度小 |
| B、pH=1时,B酸的物质的量浓度比A酸大 |
| C、B酸比A酸容易电离 |
| D、A是强碱,B是弱碱 |