题目内容
13.已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法.★还原法:在酸性介质中用FeSO4等将+6价铬还原成+3价铬.
具体流程如下:

有关离子完全沉淀的pH如表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
★电解法:将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O${\;}_{7}^{2-}$发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-;.
(5)电解法中加入氯化钠的作用是:增强溶液导电性.
分析 在酸性条件下亚铁离子将重铬酸根还原成铬离子同时生成铁离子,调节pH值,可以使铬离子和铁离子都沉淀,氢氧化铬受热分解得氧化铬,
(1)二价铁离子有还原性,Cr2O72-有强氧化性,二者能发生氧化还原反应;
(2)还原+6价铬应选用还原剂,且不能引进新的杂质;
(3)根据各种碱的性质分析判断,过氧化钠有强氧化性,钡离子和硫酸根离子能生成沉淀;根据完全沉淀对应氢氧化物的PH值判断,溶液的pH值应大于该数值;
(4)阴极上氢离子放电生成氢气;
(5)水是弱电解质,导电性能较差,氯化钠是强电解质能增强水的导电性.
解答 解:(1)二价铁离子有还原性,Cr2O72-有强氧化性,二者能发生氧化还原反应,二价铁离子被氧化成三价铁离子,Cr2O72-被还原为Cr3+,反应方程式为Cr2O72-+6Fe2++14H+═2 Cr3++6Fe3++7H2O,故答案为:Cr2O72-+6Fe2++14H+═2 Cr3++6Fe3++7H2O;
(2)能还原+6价铬,说明加入的物质有还原性,且不能引进新的杂质离子,
A.明矾没有还原性,故A错误;
B.铁屑能还原+6价铬,同时本身被氧化成三价铁离子,故B正确;
C.生石灰没有还原性,故C错误;
D.亚硫酸氢钠能还原+6价铬,同时本身被氧化成硫酸根离子,故D正确;
故答案为:BD;
(3)A.Na2O2 有强氧化性,能把Cr3+氧化成Cr6+,从而得不到Cr(OH)3,故A错误;
B.Ba(OH)2 和硫酸根离子能产生硫酸钡沉淀,生成杂质,故B错误;
C.Ca(OH)2 和 Fe3+和Cr3+产生氢氧化物沉淀,且没有其它沉淀杂质生成,故C正确;
D.NaOH使Fe3+和Cr3+产生氢氧化物沉淀,且没有其它沉淀杂质生成,故D正确;
在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀,且没有氢氧化亚铁沉淀,所以溶液的pH应大于5.6小于9,所以B正确,
故答案为:CD;B;
(4)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解,阳极上铁失电子生成二价铁离子,阴极上氢离子得电子生成氢气,电极反应式为2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-,故答案为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-;
(5)水是弱电解质,所以蒸馏水的导电能力很小,氯化钠是强电解质,在水中能完全电离导致溶液阴阳离子浓度增大,所以能增强溶液导电性,
故答案为:增强溶液导电性.
点评 本题考查了离子方程式和电极反应式的书写,难度不大,答题是注意化学用语的规范书写及工业流程原理的分析,侧重考查学生分析问题和灵活运用基础知识的能力.

 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案| A. | C2H6 | B. | C2H4 | C. | C2H2 | D. | C7H8 |
面粉酸度与面粉品质的关系表
| 面粉酸度 | <2° | 2°-4.5° | >4.5° |
| 面粉品质 | 新鲜面粉 | 陈年面粉 | 霉变面粉 |
(1)为检测某种面粉中是否含有淀粉,取一定质量的面粉放入烧杯中,加入适量的蒸馏水,搅拌,缓缓加热,溶解,取少量试液置于试管中,滴加碘液,若溶液变蓝色,就说明该面粉中含有淀粉.
(2)称取5克某种面粉放入锥形瓶,加入适量蒸馏水搅匀,为减小实验误差,现用质量分数为0.004%氢氧化钠溶液来进行测定,恰好完全反应时共消耗22毫升氢氧化钠溶液.计算该面粉的酸度4.4°;,并判断其品质(忽略两种氢氧化钠溶液密度的差异)陈年面粉.
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深.
(1)该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:白色不溶物可能为Mg(OH)2;
猜测2:白色不溶物可能为MgCO3;
猜测3:白色不溶物可能为碱式碳酸镁[yMg(OH)2•xMgCO3].
(2)为了确定产物,进行以下定性实验:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 安静燃烧,火焰呈淡蓝色 | 气体成分为氢气 |
| 实验Ⅲ | 将实验Ⅰ中的白色不溶物滤出、洗涤,取少量加入足量稀盐酸 | 产生气泡沉淀全部溶解 | 白色不溶物中含有MgCO3 |
| 实验Ⅳ | 取实验Ⅲ中的滤液,向其中加入适量CaCl2或BaCl2稀溶液 | 产生白色沉淀,溶液红色变浅 | 溶液中存在CO${\;}_{3}^{2-}$ |
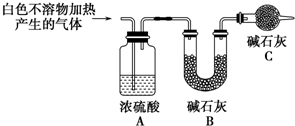
称取干燥、纯净的白色不溶物4.52g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验后装置A增重0.36g,装置B增重1.76g.
装置C的作用是防止空气中的水蒸气和CO2进入装置B中,影响实验结果;白色不溶物的化学式为Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 .
(4)写出镁与饱和碳酸氢钠溶液反应的化学方程式:3Mg+4NaHCO3+2H2O=Mg(OH)2•2MgCO3↓+2Na2CO3+3H2↑.
| A. | 该有机物分子中碳、氢、氧原子个数比为1:2:3 | |
| B. | 该有机物分子中碳、氢原子个数比为1:2 | |
| C. | 该有机物中必含氧元素 | |
| D. | 该有机物中可能不含氧元素 |




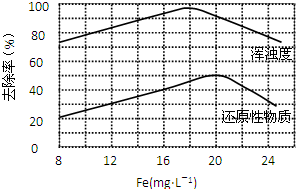 FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小.请回答下列问题:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小.请回答下列问题: