题目内容
16.将足量的SO3不断加入KOH、Ba(OH)2、KAlO2三种物质的混合溶液中,如图所示生成沉淀与加入SO3的物质的量的关系相符的图象是( )| A. | 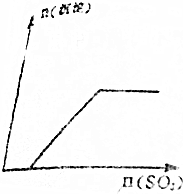 | B. | 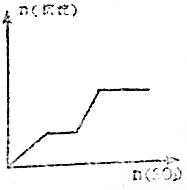 | ||
| C. | 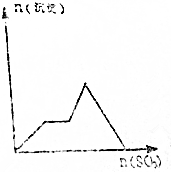 | D. |  |
分析 将足量的SO3不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,发生反应先后顺序为Ba(OH)2+SO3=BaSO4↓+H2O、2KOH+SO3=K2SO4+H2O、2KAlO2+SO3+3H2O=2Al(OH)3↓+K2SO4、2Al(OH)3+3H2SO4═Al2(SO4)3+6H2O,据此分析解答.
解答 解:将足量的SO3不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,
①先发生反应:Ba(OH)2+SO3=BaSO4↓+H2O,生成沉淀硫酸钡与通入三氧化硫的物质的量之比为1:1,
②氢氧化钡反应后再发生反应:2KOH+SO3=K2SO4+H2O,则此段沉淀的物质的量不变;
③KOH反应完全后,KAlO2与三氧化硫反应生成氢氧化铝沉淀:2KAlO2+SO3+3H2O=2Al(OH)3↓+K2SO4,生成的沉淀与三氧化硫的物质的量之比为2:1,此段曲线斜率比①大;
④最后发生反应:2Al(OH)3+3H2SO4═Al2(SO4)3+6H2O,沉淀的物质的量减小,
根据分析可知,生成沉淀与加入SO3的物质的量的关系相符的图象为D,
故选D.
点评 本题考查了混合物反应及应用,题目难度中等,明确发生反应的实质及先后顺序为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
6.下列叙述正确的是( )
| A. | 1.00mol NaCl中含有6.02×1023个NaCl分子 | |
| B. | 欲配制1.00 L 1.00mol•L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 | |
| C. | 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 | |
| D. | 电解58.5g 熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0g金属钠 |
7.下列变化需要加还原剂才能实现的是( )
| A. | MnO2→MnCl2 | B. | Fe→Fe2+ | C. | Cl-→Cl2 | D. | SO2→H2SO3 |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,5.6L O2作氧化剂时转移电子数一定为NA | |
| B. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| C. | 已知3BrF3+5H2O═HBrO3+Br2+9HF+O2↑如果有5molH2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA | |
| D. | 142gNa2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA |
10.实验室用密度为1.25g•mL-1,溶质质量分数为36.5%的浓盐酸配制
240mL 0.1mol•L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为12.5mol/L.)
(2)配制240mL 0.1mol•L-1的盐酸
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)BCAFED.
A.用30mL水洗涤2~3次,洗涤液均注入容量瓶,振荡
B.用5mL准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡、摇匀
E.改用胶头滴管加水,使溶液凹液面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是洗涤液中含有少量的溶质,为避免溶质的量的减少,应将洗涤液全部转移到容量瓶中
(5)若实验过程中出现如下情况如何处理?
①加蒸馏水时不慎超过了刻度线:重新配制.
②向容量瓶中转移溶液时不慎有液滴溅在容量瓶外面:重新配制.
(6)若实验遇到下列情况,溶液的浓度是偏高,偏低还是不变?
A.定容时仰视刻度线偏低;
B.忘记将洗涤液加入容量瓶偏低;
C.容量瓶内壁附有水珠而未干燥处理不变;
D.溶解后没有冷却便进行定容偏高.
240mL 0.1mol•L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为12.5mol/L.)
(2)配制240mL 0.1mol•L-1的盐酸
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
A.用30mL水洗涤2~3次,洗涤液均注入容量瓶,振荡
B.用5mL准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡、摇匀
E.改用胶头滴管加水,使溶液凹液面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是洗涤液中含有少量的溶质,为避免溶质的量的减少,应将洗涤液全部转移到容量瓶中
(5)若实验过程中出现如下情况如何处理?
①加蒸馏水时不慎超过了刻度线:重新配制.
②向容量瓶中转移溶液时不慎有液滴溅在容量瓶外面:重新配制.
(6)若实验遇到下列情况,溶液的浓度是偏高,偏低还是不变?
A.定容时仰视刻度线偏低;
B.忘记将洗涤液加入容量瓶偏低;
C.容量瓶内壁附有水珠而未干燥处理不变;
D.溶解后没有冷却便进行定容偏高.
8.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol丙烯酸含有NA个不饱和键 | |
| B. | 标准状况下,11.2L的苯中含有3NA个碳氢键 | |
| C. | 0.1mol/L的Na3PO4溶液中含有的阴离子总数大于0.1NA | |
| D. | 1L1.0mol/L的Na2SiO3溶液中含有的氧原子数目大于3NA |
 ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究.
ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究.