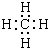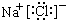��Ŀ����
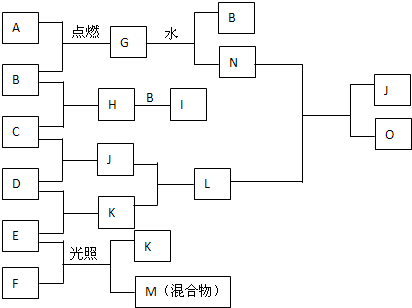
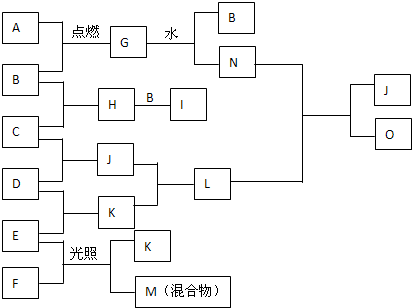
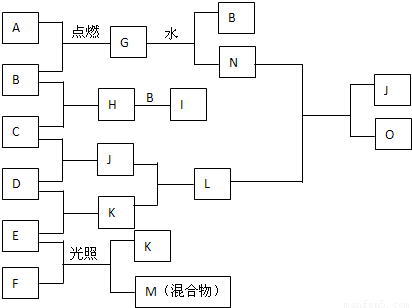
��ͼ��A��O ��ת����ϵ����֪A��һ�ֽ������ʣ�B��C��D��E��F��H��I��J��K���³�ѹ�¾�Ϊ���壬��B��C��D��E�ǵ��ʣ�I��һ�ֺ���ɫ���壬G��һ�ֵ���ɫ���壬M�ǻ����������壬J��K����������������̣���ش��������⣺
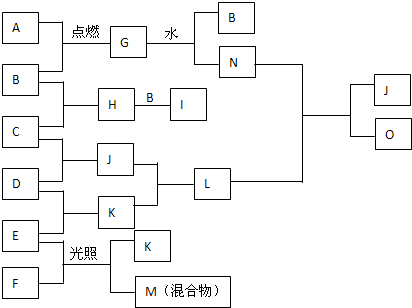
��1��д��G��ˮ��Ӧ�Ļ�ѧ����ʽ______��д������E��N��Һ��Ӧ�����ӷ���ʽ______��
��2��������G�к��еĻ�ѧ��Ϊ______��
��3��д��F�ĵ���ʽ______��������O�ĵ���ʽ______��
��4��E��F��Ӧ��������Ļ�ѧ����ʽΪ______��

��1��д��G��ˮ��Ӧ�Ļ�ѧ����ʽ______��д������E��N��Һ��Ӧ�����ӷ���ʽ______��
��2��������G�к��еĻ�ѧ��Ϊ______��
��3��д��F�ĵ���ʽ______��������O�ĵ���ʽ______��
��4��E��F��Ӧ��������Ļ�ѧ����ʽΪ______��
G��һ�ֵ���ɫ���壬���ת��G+H2O��B+N����GΪNa2O2��B�����嵥�ʣ���BΪO2��NΪNaOH��A��һ�ֽ������ʣ����A+B��G��֪��AΪNa��
I��һ�ֺ���ɫ���壬ΪNO2��BΪO2����H
I��֪HΪNO��CΪ���嵥�ʣ���B+C��H��֪��CΪN2��
J��KΪ���壬J��K����������������̣�ΪHCl��NH3����LΪNH4Cl��CΪN2��D���嵥�ʣ���ת����ϵC+D��J����JΪNH3��
KΪHCl��DΪH2����ת��D+E��K����EΪ���嵥�ʣ���EΪCl2����ת��E+F
K+M��������M�������壬��FΪ���壬���Ǽ�����������Ӧ����ת����ϵ����FΪCH4��MΪ�����±���
NΪNaOH��LΪNH4Cl����N+L��J+O����JΪNH3��OΪNaCl��
��1��GΪNa2O2����ˮ��Ӧ����������������������Ӧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2����
EΪCl2��NΪNaOH���������������Ʒ�Ӧ��Ӧ�����Ȼ��ơ��������ơ�ˮ����Ӧ���ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����Cl2+2OH-=Cl-+ClO-+H2O��
��2��Na2O2�����ӻ���������������������֮���γ����Ӽ�����������������ԭ��֮���γɹ��ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��3��FΪCH4��������̼ԭ������ԭ��֮���γ�1�Թ��õ��Ӷԣ�����ʽΪ��
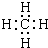
��
OΪNaCl�������ӻ�������������������ӹ��ɣ�����ʽΪ��
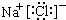
���ʴ�Ϊ��
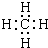
��
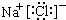
��
��4���ȴ�������һ�ȼ���������E��F��Ӧ��������ķ�Ӧ�Ǽ�����������Ӧ����һ�ȼ������Ȼ��⣬��Ӧ��Ӧ����ʽΪCH4+Cl2
CH3Cl+HCl��
�ʴ�Ϊ��CH4+Cl2
CH3Cl+HCl��
I��һ�ֺ���ɫ���壬ΪNO2��BΪO2����H
| B |
J��KΪ���壬J��K����������������̣�ΪHCl��NH3����LΪNH4Cl��CΪN2��D���嵥�ʣ���ת����ϵC+D��J����JΪNH3��
KΪHCl��DΪH2����ת��D+E��K����EΪ���嵥�ʣ���EΪCl2����ת��E+F
| ���� |
NΪNaOH��LΪNH4Cl����N+L��J+O����JΪNH3��OΪNaCl��
��1��GΪNa2O2����ˮ��Ӧ����������������������Ӧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2����
EΪCl2��NΪNaOH���������������Ʒ�Ӧ��Ӧ�����Ȼ��ơ��������ơ�ˮ����Ӧ���ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����Cl2+2OH-=Cl-+ClO-+H2O��
��2��Na2O2�����ӻ���������������������֮���γ����Ӽ�����������������ԭ��֮���γɹ��ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��3��FΪCH4��������̼ԭ������ԭ��֮���γ�1�Թ��õ��Ӷԣ�����ʽΪ��
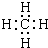
��
OΪNaCl�������ӻ�������������������ӹ��ɣ�����ʽΪ��
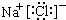
���ʴ�Ϊ��
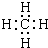
��
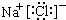
��
��4���ȴ�������һ�ȼ���������E��F��Ӧ��������ķ�Ӧ�Ǽ�����������Ӧ����һ�ȼ������Ȼ��⣬��Ӧ��Ӧ����ʽΪCH4+Cl2
| ���� |
�ʴ�Ϊ��CH4+Cl2
| ���� |

��ϰ��ϵ�д�
�����Ŀ
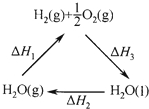 ���ڿ�ѧ������Ѱ��̫����ת���ɻ�ѧ�ܣ����а취֮һ��������̫���ܽ�H2O�ֽ��H2���ٽ���ѧ��ת��Ϊ������Դ����ͼ���йص�����ѭ��ʾ��ͼ�������й�˵����ȷ���ǣ�������
���ڿ�ѧ������Ѱ��̫����ת���ɻ�ѧ�ܣ����а취֮һ��������̫���ܽ�H2O�ֽ��H2���ٽ���ѧ��ת��Ϊ������Դ����ͼ���йص�����ѭ��ʾ��ͼ�������й�˵����ȷ���ǣ�������| A��ͼ�С�H1=��H2+��H3 | B�����H-H�ļ���Ϊa kJ/mol��o=o����Ϊb kJ/mol����Ͽ�1mol H-O������Ҫ��̫����Ϊ����H1+a+b��kJ | C��H2ȼ����Ϊ��H3 kJ/mol | D��ˮ���������е�������Һ̬ˮ���H2 kJ |