题目内容
下列表示化学反应的离子方程式正确的是
A.Na2O2与水反应:Na2O2 + H2O = 2Na+ + 2OH- + O2↑
B.用惰性电极电解MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.Ba(OH)2溶液中加入过量的NaHSO4溶液:Ba2++SO42-+OH-+H+=BaSO4↓+H2O
D.硫酸亚铁溶液中加入酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O
D
【解析】
试题分析:A.反应方程式为配平,Na2O2与水反应:2Na2O2 +2 H2O = 4Na+ + 4OH- + O2↑,错误;B、用惰性电极电解MgCl2溶液:2Cl-+Mg2++2H2O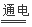 Mg(OH)2↓+H2↑+Cl2↑,错误;C、Ba(OH)2溶液中加入过量的NaHSO4溶液,应该以Ba(OH)2溶液为标准,离子方程式是:Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O,错误;D、硫酸亚铁溶液中加入酸化的双氧水,发生氧化还原反应,Fe2+被氧化为Fe3+,离子方程式是:2Fe2++2H++H2O2=2Fe3++2H2O,正确。
Mg(OH)2↓+H2↑+Cl2↑,错误;C、Ba(OH)2溶液中加入过量的NaHSO4溶液,应该以Ba(OH)2溶液为标准,离子方程式是:Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O,错误;D、硫酸亚铁溶液中加入酸化的双氧水,发生氧化还原反应,Fe2+被氧化为Fe3+,离子方程式是:2Fe2++2H++H2O2=2Fe3++2H2O,正确。
考点:考查离子方程式书写的正误判断的知识。

一定温度下,难溶强电解质的饱和溶液中存在着沉淀溶解平衡,其平衡常数为
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25℃) | 8.0×10﹣16 | 2.2×10﹣20 | 4.0×10﹣38 |
对于含Fe2(SO4)3、FeSO4和CuSO4各0.5mol的混合溶液1L,根据上表数据判断,说法错误的是
A.向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B.向溶液中加入双氧水,并用CuO粉末调节pH,过滤后可获较纯净的CuSO4溶液
C.该溶液中c(SO42﹣):[c(Fe3+)+c(Fe2+)+c(Cu2+)]=5:4
D.将少量FeCl3粉末加入含Cu(OH) 2的悬浊液中,其中c(Cu2+)增大




 和②
和② ,M的结构简式为 。
,M的结构简式为 。