题目内容
20.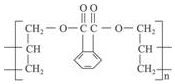 DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )
DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )①烯CH2=CH2
②丙烯CH3CH=CH2
③丙烯醇(CH2=CH-CH2OH)
④邻苯二甲酸
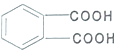
⑤邻苯二甲酸酯
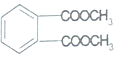
| A. | ①② | B. | ③④ | C. | ②④ | D. | ③⑤ |
分析 有机物含有酯基,应由酸和醇发生酯化反应,对应的单质分别含有羟基、羧基,且为二元酸,链节中主碳链为2个碳原子,对应的单体含有碳碳双键,以此解答该题.
解答 解:按如图 所示断键后,氧原子接H原子,碳原子接-OH,再将两端的半键连接成双键,所以可得单体为
所示断键后,氧原子接H原子,碳原子接-OH,再将两端的半键连接成双键,所以可得单体为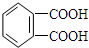 和CH2=CH-CH2-OH,
和CH2=CH-CH2-OH,
故选B
点评 本题考查高分子化合物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意根据链节判断高聚物是加聚、还是缩聚而成是关键,注意理解结合反应的机理,难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
20.已知常温下浓度为0.1mol/L的几种溶液的pH如表.下列有关说法正确的是( )
| 溶质 | pH |
| NaF | 7.5 |
| Na2CO3 | 11.6 |
| NaClO | 9.7 |
| NaHCO3 | 8.3 |
| A. | 同温度同浓度下,酸由强到弱的顺序为:HF>H2CO3>HClO | |
| B. | 水解方程式:F-+H2O?HF+OH-的平衡常数为1×10-13 | |
| C. | 将CO2通入0.lmol/LNa2CO3溶液至溶液呈中性,则溶液中:2c(CO32-)+c(HCO3-)=0.1mol/L | |
| D. | 等物质的量的NaF和HF混合溶液中粒子浓度大小关系为:c(HF)>c(Na+)>c(F-)>c (H+)>c(OH-) |
11. (1)用“=”、“>”、“<”填写下表
(1)用“=”、“>”、“<”填写下表
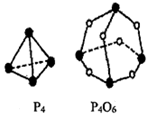
(2)白磷(P4)和P4O6的分子结构如图,现提供以下化学键的键能:P-P为E1 kJ•mol-1、P-O为E2 kJ•mol-1、O=O为E3 kJ•mol-1,则:
P4(s)+3O2(g)═P4O6(s)的反应热△H=(6E1+3E3-12E2)kJ•mol-1(用E1、E2、E3表示)
 (1)用“=”、“>”、“<”填写下表
(1)用“=”、“>”、“<”填写下表 | 第一电离能 | 电负性 | 晶格能 | 沸点 |
| O <N | Cl <F | NaCl >KBr | HF >HCl |
P4(s)+3O2(g)═P4O6(s)的反应热△H=(6E1+3E3-12E2)kJ•mol-1(用E1、E2、E3表示)
8. A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )
A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )
 A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )
A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )| A. | B 的M层电子数是K层的3倍 | |
| B. | C 的离子具有与 Na+相同的电子层结构 | |
| C. | A 与 D 形成的化合物属于离子化合物 | |
| D. | C 的简单阴离子比 D 的简单阴离子还原性强 |
15.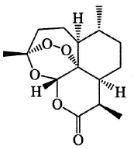 中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
 中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖.青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )| A. | 提取过程中为防止破坏青蒿素结构,应避免高温,故采用低沸点溶剂乙醚进行萃取 | |
| B. | 可使用质谱仪测出这个分子的相对分子质量,也可用紫外光谱确定这个分子的环状结构 | |
| C. | 青蒿素是脂溶性的,既可看作是醚类也可看作是酯类,既有氧化性又有还原性 | |
| D. | 元素分析仪可以确定青蒿素中是否含有C、H、O等元素 |
12.下列化工生产涉及的变化主要是物理变化的是( )
| A. | 煤的干馏 | B. | 石油的分馏 | C. | 石油的裂化 | D. | 石油的裂解 |
9.某同学设计了如下实验测量mg铜银合金样品中铜的质量分数:
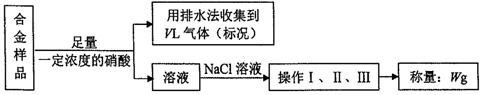
下列说法中不正确的是( )

下列说法中不正确的是( )
| A. | 铜、银都能与硝酸反应,收集到的VL气体全为NO | |
| B. | 操作I、II、III分别为过滤、洗涤、干燥 | |
| C. | 利用气体体积VL及样品质量mg可计算铜的质量分数 | |
| D. | 久置的银器变黑、铜绿的形成都发生了氧化还原反应 |
10.化学与生产、生活、科技、环境等密切相关,下列说法正确的是( )
| A. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| B. | 铅笔芯的原材料为铅,所以儿童常咬铅笔头容易铅中毒 | |
| C. | 网络飞速发展,得益于光纤良好的导电性,光纤的主要成分是二氧化硅 | |
| D. | 用K2FeO4取代Cl2处理饮用水,不仅可杀菌消毒,同时还能沉降水中的悬浮物 |
 .
. .
.