题目内容
下列说法正确的是( )
| A、除去MgCl2溶液中混有少量AlCl3,用氨水和盐酸 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、金属原子只有还原性,金属阳离子只有氧化性 |
| D、用滴管滴加液体时,为防止液滴溅出,滴管紧贴试管内壁 |
考点:物质的分离、提纯的基本方法选择与应用,氧化还原反应,电解质与非电解质,强电解质和弱电解质的概念,计量仪器及使用方法
专题:
分析:A.加入氨水,引入新杂质;
B.结合非电解质、强电解质和弱电解质的定义判断;
C.Fe2+等离子具有还原性;
D.滴加液体时应防止污染药品.
B.结合非电解质、强电解质和弱电解质的定义判断;
C.Fe2+等离子具有还原性;
D.滴加液体时应防止污染药品.
解答:
解:A.加入氨水,生产氯化铵,引入新杂质,故A错误;
B.蔗糖溶液不能导电,为非电解质,硫酸钡难溶于水,但能完全电离,为强电解质,水部分电离,为弱电解质,故B正确;
C.Fe2+等离子具有还原性,故C错误;
D.滴管的使用:竖直悬空,不能伸入试管内部,防止污染药品,故D错误.
故选B.
B.蔗糖溶液不能导电,为非电解质,硫酸钡难溶于水,但能完全电离,为强电解质,水部分电离,为弱电解质,故B正确;
C.Fe2+等离子具有还原性,故C错误;
D.滴管的使用:竖直悬空,不能伸入试管内部,防止污染药品,故D错误.
故选B.
点评:本题涉及物质的分类、电解质的概念和分类以及实验基本操作知识,属于综合知识的考查题,要求学生具有分析和解决问题的能力,难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
根据原子结构及元素周期律的知识,下列推断正确的是( )
A、
| ||||
| B、同主族元素含氧酸的酸性随核电荷数的增加而减弱 | ||||
| C、同周期元素(除0族元素外)从左到右,原子半径逐渐减小 | ||||
| D、若M+和R2-的核外电子层结构相同,则原子序数R>M |
下列说法中正确的是( )
| A、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| B、需要加热的化学反应,生成物的总能量一定高于反应物的总能量 |
| C、熵减的反应一定是非自发反应 |
| D、己知2C(s)+2O2(g)=2CO2(g)△H1,2C(s)+O2(g)=2CO(g)△H2,则△H1<△H2 |
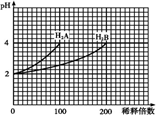 常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述不正确的是( )
常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述不正确的是( )| A、H2A为二元强酸 |
| B、pH=4的NaHA水溶液中离子浓度大小为:c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-) |
| C、含NaHA、NaHB的混合溶液中,离子浓度大小为:c(Na+)=c(A2-)+c(HB-)+c(B2-)+c(H2B) |
| D、Na2B的水溶液中,离子浓度大小为:c(Na+)>c(B2-)>c(OH-)>c(H+) |
下列关于核外电子的描述中,正确的是( )
| A、电子云图中一个小黑点表示一个电子 |
| B、电子式中元素符号周围的小黑点数表示核外电子总数 |
| C、s电子在s电子云的球形空间内做规则运动 |
| D、核外电子的能量大小主要是由电子层和电子亚层决定 |
室温下,将一元酸HA溶液和NaOH溶液等体积混合(忽略体积变化),实验数据如下表下列判断正确的是( )
| 实验编号 | 起始浓度(mol/L) | 反应后溶液的pH | |
| C(HA) | C(NaOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
| A、实验①反应后的溶液中C(Na+)>C(A-)>C(OH-)>C(H+) | ||
B、实验①反应后的溶液中C(OH-)=C(Na+)-C(A-)=
| ||
| C、实验②反应后的溶液中C(A-)+C(HA)=0.1 mol/L | ||
| D、实验②反应后的溶液中C(Na+)=C(A-)>C(OH-)=C(H+) |
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏低的原因是( )
| A、定容时俯视液面 |
| B、转移溶液前溶液未冷却至室温 |
| C、容量瓶未干燥 |
| D、未洗涤烧杯和玻璃棒 |
下列关于判断过程方向的说法正确的是( )
| A、光合作用是自发反应 |
| B、所有自发进行的化学反应都是放热反应 |
| C、相同物质的量的同一物质在固、液、气三种状态时的熵值相同 |
| D、由能量判据和熵判据组合而成的复合判据,将更适合所有的过程 |