题目内容
(1)阿司匹林( )具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式:
)具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式:
(2)一种缓释阿司匹林的结构式如图:
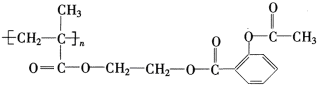
该物质在酸性条件下水解生成阿司匹林、 和一种聚合物.这种聚合物的单体的结构简式是 .
 )具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式:
)具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式:(2)一种缓释阿司匹林的结构式如图:
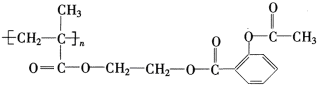
该物质在酸性条件下水解生成阿司匹林、
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:(1)阿司匹林中-COOH、-COOC-及水解生成的酚-OH均与NaOH反应;
(2)酸性条件下水解生成阿司匹林、乙二醇和一种聚合物,聚合物为聚2-甲基丙烯酸,则单体为2-甲基丙烯酸.
(2)酸性条件下水解生成阿司匹林、乙二醇和一种聚合物,聚合物为聚2-甲基丙烯酸,则单体为2-甲基丙烯酸.
解答:
解:(1)阿司匹林中-COOH、-COOC-及水解生成的酚-OH均与NaOH反应,该反应为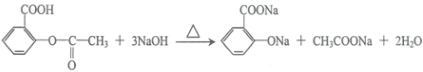 ,
,
故答案为: ;
;
(2)在酸性条件下水解生成阿司匹林、乙二醇和一种聚合物,聚合物为聚2-甲基丙烯酸,则单体为2-甲基丙烯酸,其结构简式为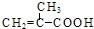 ,
,
故答案为:乙二醇;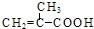 .
.
 ,
,故答案为:
 ;
;(2)在酸性条件下水解生成阿司匹林、乙二醇和一种聚合物,聚合物为聚2-甲基丙烯酸,则单体为2-甲基丙烯酸,其结构简式为
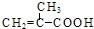 ,
,故答案为:乙二醇;
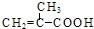 .
.
点评:本题考查有机物的结构与性质,为高考常见题型,把握阿司匹林结构中官能团、性质的关系为解答的关键,(2)为解答的难点,题目难度中等.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
下列有关物质性质的比较中,正确的是( )
①热稳定性:CH4>NH3>H2O
②还原性:I->Br->Cl-
③酸性:H3PO4>H2SO4>HClO4
④沸点:HI>HBr>HCl>HF.
①热稳定性:CH4>NH3>H2O
②还原性:I->Br->Cl-
③酸性:H3PO4>H2SO4>HClO4
④沸点:HI>HBr>HCl>HF.
| A、①③ | B、②④ | C、①④ | D、只有② |
下列说法正确的是( )
| A、白磷分子呈正四面体,键角109°28′,1mol白磷含共价键6mol |
| B、臭氧分子呈直线型,等质量的臭氧和氧气所含的氧原子数相同 |
| C、S8是分子晶体,8个硫原子在同一个平面上,摩尔质量为256g |
| D、石墨晶体呈层状结构,每个碳原子只有3个价电子形成共价键 |
下列实验与所得结论相符的是( )
| A、将碘水倒入分液漏斗,加适量乙醇,震荡后静置,能将碘萃取到乙醇中 |
| B、用湿润的pH试纸测定溶液的pH,测定结果偏小,该溶液一定呈酸性 |
| C、向某溶液中加入K3[Fe(CN)6]溶液,生成特征蓝色的沉淀,原溶液中含有Fe2+ |
| D、在含有FeCl2杂质的FeCl3溶液中通入足量的Cl2后,充分加热蒸干,可得到纯净的FeCl3 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol N2所含有的原子数为NA |
| B、标准状况下,22.4 L水中含有的水分子数为NA |
| C、标准状况下,22.4 L氯化氢所含的原子数为NA |
| D、32 g O2所含的氧原子数目为2NA |
关于反应2NaBr+Cl2═2NaCl+Br2,下列说法不正确的是( )
| A、Cl2是氧化剂,反应中Cl原子得到电子 |
| B、当1molCl2完全反应时,有2mol电子发生转移 |
| C、NaBr是还原剂,反应中溴离子得到电子 |
| D、当1molNaBr完全反应时,有1mol电子发生转移 |
升高温度,下列数据不一定增大的是( )
| A、化学反应速率v |
| B、水的离子积常数Kw |
| C、化学平衡常数K |
| D、弱酸的电离平衡常数Ki |
化学已渗透到人类生活的各个方面.下列说法不正确的是( )
| A、人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
| B、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| C、地球上CH4、CO2等气体含量上升容易导致温室效应加剧,进而引发灾难性气候 |
| D、禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |