题目内容
某学生用氯气杀菌漂白的自来水配制下列物质的溶液,不会产生明显药品变质的是( )
| A、石蕊 |
| B、AlCl3 |
| C、NaOH |
| D、AgNO3 |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:自来水常用氯气消毒,往往含有Cl2、Cl-、HClO、ClO-、H+等粒子,用自来水配制药品时,若不与自来水中的粒子反应,则不变质,否则变质.
解答:
解:A.自来水中含有Cl2、HClO、ClO-等物质,可氧化石蕊而导致石蕊变质,并且H+也可使石蕊变质,故A错误;
B.氯化铝与自来水中的Cl2、Cl-、HClO、ClO-、H+等粒子不反应,不变质,故B正确;
C.自来水中含有Cl2、HClO、H+等物质,均可与NaOH反应而导致溶液变质,故C错误;
D.自来水中含有Cl-,与硝酸银反应生成AgCl沉淀而导致硝酸银变质,故D错误.
故选B.
B.氯化铝与自来水中的Cl2、Cl-、HClO、ClO-、H+等粒子不反应,不变质,故B正确;
C.自来水中含有Cl2、HClO、H+等物质,均可与NaOH反应而导致溶液变质,故C错误;
D.自来水中含有Cl-,与硝酸银反应生成AgCl沉淀而导致硝酸银变质,故D错误.
故选B.
点评:本题考查氯水的组成和性质,题目难度不大,注意把握氯水的成分以及相关物质的性质,判断可能发生的反应.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
下列物质中,能用酸性高锰酸钾溶液鉴别的是( )
| A、乙烯、乙炔 |
| B、1-己烯 甲苯 |
| C、苯 正己烷 |
| D、苯 2-丁炔 |
有关化工生产原理说法正确的是( )
A、工业上制粗硅:SiO2+C
| ||||
B、海水提镁的主要步骤为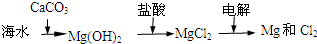 | ||||
C、海水提溴原理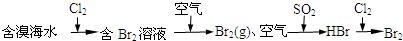 | ||||
| D、硫酸工业的接触室、合成氨工业的合成塔和氯碱工业的电解槽都有热交换器 |
在实验室中,对下列事故或药品的处理正确的是( )
| A、漂白粉长期放置在烧杯中 |
| B、金属钠着火燃烧时,不能用泡沫灭火器灭火,应该用沙子灭火 |
| C、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| D、有大量的氯气泄漏时,用碳酸钠溶液浸湿软布蒙面,并迅速离开现场 |
已知乙烯分子是平面结构,因此,1,2-二氯乙烯可以形成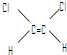 和
和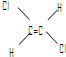 两种不同的空间异构体.下列各物质中,能形成类似上述两种空间异构体的是( )
两种不同的空间异构体.下列各物质中,能形成类似上述两种空间异构体的是( )
 和
和 两种不同的空间异构体.下列各物质中,能形成类似上述两种空间异构体的是( )
两种不同的空间异构体.下列各物质中,能形成类似上述两种空间异构体的是( )| A、1-丁烯 | B、丙烯 |
| C、2-甲基-2-丁烯 | D、2─丁烯 |
 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)