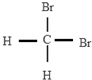
题目内容
2.Cu片放入0.1 mol•L-1FeCl3溶液中,反应一定时间后取出Cu片,测得溶液中Fe3+和Fe2+的物质的量浓度为:c(Fe3+):c(Fe2+)=2:3,则溶液中Cu2+与Fe3+的物质的量之比为( )| A. | 3:2 | B. | 3:5 | C. | 3:4 | D. | 4:3 |
分析 先利用假设法求出二价铁离子、三价铁离子的物质的量,再根据离子方程式中铜离子和二价铁离子的关系求出铜离子的物质的量.
解答 解:将Cu片放入FeCl3溶液中.发生反应:Cu+2Fe3+=Cu2++2Fe2+,假设溶液中n(Fe2+)=3mol,则溶液中n(Fe3+)=2mol,
由离子方程式可知,n(Cu2+)=$\frac{1}{2}$n(Fe2+)=$\frac{1}{2}$×3mol=1.5mol,所以n(Cu2+):n(Fe3+)=1.5mol:2mol=3:4,
故选C.
点评 本题考查的是铜的化学性质、离子方程式的有关计算,巧妙利用假设法是解本题的关键.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
3.下列反应属于氧化还原反应的是( )
①Na2O2+2H2O═2NaOH+H2O2
②IBr+H2O═HIO+HBr
③Cr2O72-+4H2O2+2H+═2CrO5+5H2O(CrO5的结构为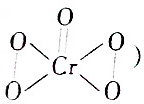 )
)
①Na2O2+2H2O═2NaOH+H2O2
②IBr+H2O═HIO+HBr
③Cr2O72-+4H2O2+2H+═2CrO5+5H2O(CrO5的结构为
 )
)| A. | ①②③ | B. | ② | C. | ③ | D. | 都不是 |
10.下列指定微粒的数目相等的是( )
| A. | 等物质的量的CaCl2和CaO2含有的离子数 | |
| B. | 等质量的水与重水含有的电子数 | |
| C. | 同温、同压同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别与足量氯气完全反应时转移的电子数 |
7.常温下,将0.1000mol•L-1 NaOH溶液滴入20.00mL 0.1000mol•L-1的一元酸HA溶液中,测得混合溶液的pH变化曲线如图所示.下列说法正确的是( )

| A. | ①点所示溶液中:c(A-)+c(OH-)=c(HA)+c(H+) | |
| B. | ②点所示溶液中:c(Na+)>c(HA)>c(A-)>c(H+)>c(OH-) | |
| C. | ②点所示溶液中:2c(Na+)=c(HA)+c(A-) | |
| D. | ③点所示滴入的NaOH溶液的体积V>20.00 mL |
14.下列变化不属于化学变化的是( )
| A. | 石油分馏 | B. | 煤的干馏 | C. | 钢铁生锈 | D. | 煤的液化 |
11.下列实验方法能达到实验目的是( )
| A. | 用排水集气法收集氨气 | |
| B. | 用分液漏斗分离水与乙醇的混合物 | |
| C. | 用淀粉溶液检验溶液中是否存在碘单质 | |
| D. | 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液 |
12.将溶质的质量分数为14%的KOH溶液加热蒸发掉100g水后,得到溶质的质量分数为28%的溶液80mL,此时溶液的物质的量浓度为( )
| A. | 5 mol/L | B. | 6.25 mol/L | C. | 7 mol/L | D. | 6.75 mol/L |
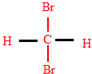 和
和