题目内容
常温下测得某无色溶液中由水电离出c(H+)为10-13mol/L,该溶液中一定能大量共存的离子组是( )
| A、K+、Na+、Cl-、CO32- |
| B、K+、Na+、NO3-、SO42- |
| C、Mg2+、K+、NO3-、Cl- |
| D、Fe2+、NO3-、SO42-、NH4+ |
考点:离子共存问题
专题:离子反应专题
分析:常温下测得某无色溶液中由水电离出c(H+)为10-13mol/L,抑制水电离,则溶液中的溶质为酸或碱,溶液无色说明不含有颜色的离子,如铜离子、铁离子、高锰酸根离子等.
解答:
解:A.如果溶液呈酸性,则氢离子和碳酸根离子反应生成二氧化碳和水,所以这几种离子不一定能大量共存,故A错误;
B.这几种离子之间不反应且和氢离子或氢氧根离子也不反应,所以能大量共存,故B正确;
C.镁离子和氢氧根离子反应生成氢氧化镁沉淀,所以该溶液中这几种离子不一定能大量共存,故C错误;
D.碱性条件下不能大量存在铵根离子,酸性条件下,亚铁离子和硝酸根离子发生氧化还原反应而不能大量共存,故D错误;
故选B.
B.这几种离子之间不反应且和氢离子或氢氧根离子也不反应,所以能大量共存,故B正确;
C.镁离子和氢氧根离子反应生成氢氧化镁沉淀,所以该溶液中这几种离子不一定能大量共存,故C错误;
D.碱性条件下不能大量存在铵根离子,酸性条件下,亚铁离子和硝酸根离子发生氧化还原反应而不能大量共存,故D错误;
故选B.
点评:本题考查离子共存,为高考高频点,侧重考查复分解反应及氧化还原反应,明确离子共存条件即可解答,易错选项是D,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
在甲、乙、丙、丁四个烧杯内分别放入0.1molNa、Na2O、Na2O2、NaOH,然后各加入100ml水,搅拌后固体完全溶解,则甲、乙、丙、丁所得溶液的质量分数大小顺序为( )
| A、甲∠乙∠丙∠丁 |
| B、丁∠甲∠丙=乙 |
| C、甲=丁∠丙=乙 |
| D、丁∠甲∠乙∠丙 |
化学在生产和日常生活中有着重要的应用.下列说法正确的是( )
| A、电解MgCl2饱和溶液,可制得金属镁 |
| B、用食醋去除水壶中的水垢所发生的是水解反应 |
| C、在海轮外壳上镶入不活泼的铜块,可减缓船体的腐蚀速率 |
| D、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用作净化剂 |
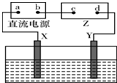 如图,Z为浸透饱和食盐水和酚酞试液的滤纸,水槽中盛有足量CuSO4溶液,X、Y为石墨电极.接通电路后,发现Z上的d点显红色.下列说法正确的是( )
如图,Z为浸透饱和食盐水和酚酞试液的滤纸,水槽中盛有足量CuSO4溶液,X、Y为石墨电极.接通电路后,发现Z上的d点显红色.下列说法正确的是( )| A、接通电路后,水槽中溶液的pH不变 |
| B、b是正极,Y电极上发生氧化反应 |
| C、同温同压下,X、Y两电极上产生气体的体积相等 |
| D、d点显红色是因为接通电路后OH-向d点移动 |
下列物质的检验,其结论一定正确的是( )
| A、某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明该溶液中一定含有SO42- |
| B、某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 CO32-或 HCO3- |
| C、某溶液中加盐酸产生刺激性气味的无色气体,该气体能使品红溶液褪色,说明该溶液中一定含有SO32- |
| D、取少量久置的Na2SO3样品于试管中加水溶解,再加入足量盐酸有气体产生,然后加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
H+浓度均为0.01mol/L的盐酸和醋酸各100ml分别稀释2倍后,再分别加入足量的锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A、盐酸和醋酸分别与锌反应放出的氢气一样多 |
| B、醋酸与锌反应放出氢气多 |
| C、醋酸与锌反应速率相等 |
| D、盐酸和醋分别与锌反应的速度一样大 |

 如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末.回答下列问题.
如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末.回答下列问题.